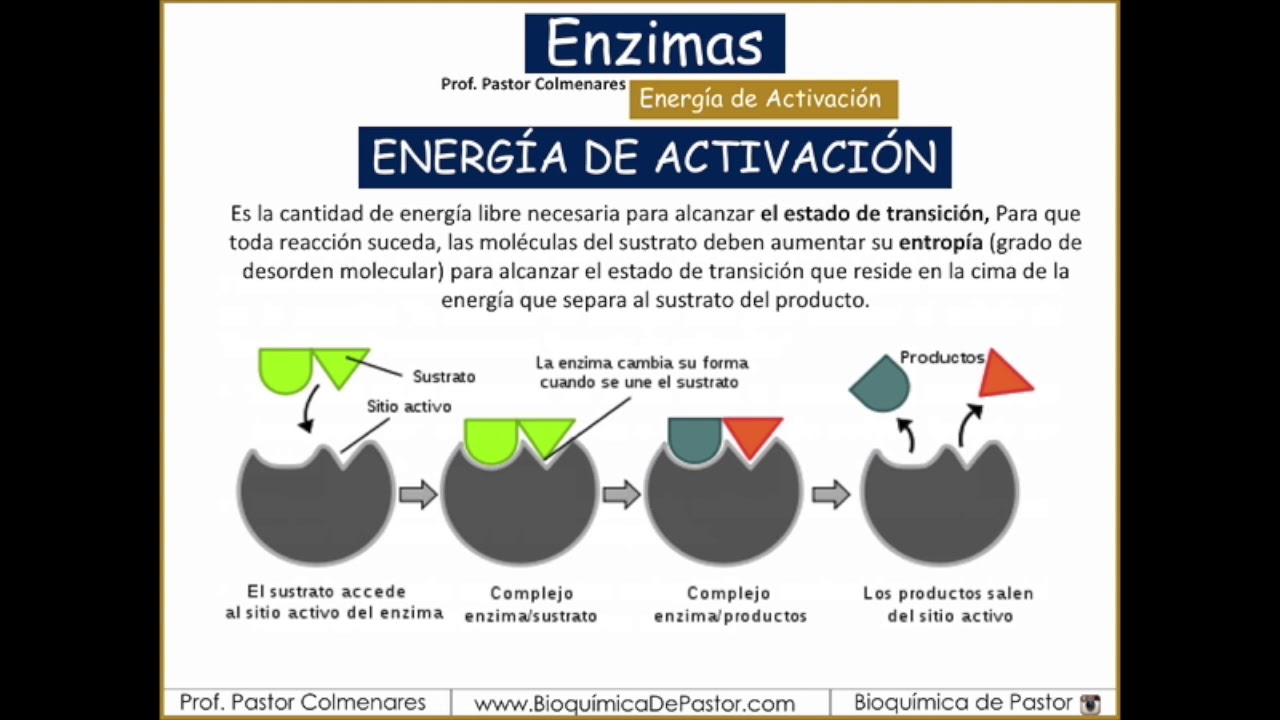
Las ENZIMAS y la ENERGÍA DE ACTIVACIÓN
Summary
TLDREste vídeo explica cómo las enzimas, que pueden ser ARN o proteínas, actúan como catalizadores biológicos aumentando la velocidad de reacciones químicas en sistemas vivos. Se discute la teoría de la 'llave y cerradura' de Emil Fischer, y cómo la flexibilidad y la interacción del sitio activo de las enzimas con los sustratos es crucial para su función. Además, se menciona la importancia de la energía de activación y cómo las enzimas la disminuyen para facilitar reacciones, así como el papel de los cofactores en la actividad enzimática.
Takeaways
- 🔬 Los sistemas vivos pueden realizar diversas transformaciones químicas, gracias principalmente a las enzimas.
- 🧬 La mayoría de las enzimas son proteínas globulares grandes formadas por cadenas polipeptídicas.
- 🔑 Las enzimas tienen un sitio activo donde se unen los sustratos, similar a un modelo llave-cerradura.
- ⚙️ Las enzimas funcionan como catalizadores biológicos, acelerando reacciones sin cambiar químicamente.
- ⏳ Una sola enzima puede catalizar miles de reacciones en segundos, lo que las hace muy efectivas en pequeñas cantidades.
- 🎯 Las enzimas tienen una especificidad muy alta, solo aceleran un tipo de reacción en medio de muchas otras.
- 🔧 El modelo de ajuste inducido sugiere que las enzimas cambian su conformación para encajar mejor con los sustratos.
- ⚡ La energía de activación es la barrera energética que los reactivos deben superar para que ocurra una reacción.
- 🔥 La temperatura y la concentración de los reactivos influyen en cuántas moléculas alcanzan la energía de activación.
- 🧲 Algunas enzimas necesitan cofactores, como iones o coenzimas, para poder funcionar adecuadamente en reacciones químicas.
Q & A
¿Qué son los sistemas vivos y qué son capaces de realizar?
-Los sistemas vivos son capaces de llevar a cabo la mayoría de los tipos de transformaciones químicas conocidas.
¿Cuál es el papel fundamental de las enzimas en los sistemas vivos?
-Las enzimas son esenciales en los sistemas vivos ya que son las moléculas que catalizan las reacciones químicas permitiendo que estos sistemas realicen sus funciones vitales.
¿Cuál es la mayoría de las enzimas en términos de su composición molecular?
-La mayoría de las enzimas son proteínas globulares de gran tamaño, formadas por una o más cadenas polipeptídicas.
¿Cómo se describe la estructura de las enzimas y su relación con el sustrato?
-Las enzimas tienen una estructura que se plega formando un surco o bolsillo, conocido como el sitio activo, donde las moléculas del sustrato se encajan y se producen las reacciones.
¿Cómo funcionan las enzimas como transductores energéticos?
-Las enzimas pueden capturar energía de diferentes tipos, como la energía química o luminosa, y almacenarla en su estructura. Posteriormente, liberan esa energía para realizar trabajo útil, como impulsar reacciones químicas.
¿Qué es un catalizador biológico y cómo lo son las enzimas?
-Un catalizador biológico es una sustancia que modifica la velocidad de una reacción química sin sufrir un cambio químico permanente. Las enzimas son catalizadores biológicos que interactúan con sus sustratos con alta especificidad.
¿Qué es el modelo de la 'llave y cerradura' en relación con las enzimas y por qué fue cuestionado?
-El modelo de la 'llave y cerradura' es una teoría que describe cómo el sustrato se ajusta perfectamente al sitio activo de la enzima, como una llave en una cerradura. Sin embargo, estudios posteriores sugieren que el sitio activo es más flexible e interactivo, lo que cuestiona esta analogía.
¿Qué es la energía de activación y cómo está relacionada con la temperatura y la concentración de los reactivos?
-La energía de activación es la diferencia de energía libre entre los reactivos y sus estadios intermedios. A mayor temperatura y concentración de reactivos, mayor será la cantidad de átomos o moléculas que alcance la energía de activación, lo que incrementa la velocidad de la reacción.
¿Cómo disminuyen las enzimas la energía de activación de las reacciones?
-Las enzimas disminuyen la energía de activación formando asociaciones temporales transitorias con las moléculas que reaccionan, acercándose a ellas y debilitando los enlaces químicos existentes, lo que facilita la formación de nuevos enlaces.
¿Qué son los cofactores y cuál es su papel en la función de las enzimas?
-Los cofactores son sustancias adicionales, ya sean iones o moléculas orgánicas de bajo peso molecular, que son necesarias para que algunas enzimas funcionen. Aportan funciones específicas, como la transferencia de grupos químicos o la transferencia de electrones.
¿Qué es el di nucleótido de nicotinamida y adenina y cuál es su importancia?
-El di nucleótido de nicotinamida y adenina es un cofactor que desempeña un papel fundamental en procesos como la glucólisis y la respiración celular, ya que a menudo actúa como un sector de electrones en reacciones de óxido-reducción.
Outlines

Cette section est réservée aux utilisateurs payants. Améliorez votre compte pour accéder à cette section.
Améliorer maintenantMindmap

Cette section est réservée aux utilisateurs payants. Améliorez votre compte pour accéder à cette section.
Améliorer maintenantKeywords

Cette section est réservée aux utilisateurs payants. Améliorez votre compte pour accéder à cette section.
Améliorer maintenantHighlights

Cette section est réservée aux utilisateurs payants. Améliorez votre compte pour accéder à cette section.
Améliorer maintenantTranscripts

Cette section est réservée aux utilisateurs payants. Améliorez votre compte pour accéder à cette section.
Améliorer maintenant5.0 / 5 (0 votes)