Der Reaktionsquotient Q - Die Reaktionsrichtung vorraus sagen
Summary
TLDRIn diesem Video wird der Reaktionsquotient QC und sein Zusammenhang mit der Gleichgewichtskonstante KC erläutert. Es wird erklärt, wie man mit QC vorhersagen kann, ob die Reaktion zu einem bestimmten Zeitpunkt noch abläuft und in welche Richtung sich die Konzentration der Produkte oder Edukte verändert. Anschauliche Beispiele, wie die Bildung von Jodwasserstoff, helfen das Konzept zu verdeutlichen. Ein Vergleich zwischen QC und KC zeigt, ob mehr Produkte oder Edukte entstehen. Das Video bietet hilfreiche Einblicke in chemische Reaktionsgleichgewichte und gibt Tipps zur Berechnung von QC.
Takeaways
- 📊 Der Reaktionsquotient QC zeigt das Verhältnis der Konzentrationen von Produkten und Edukten zu einem bestimmten Zeitpunkt an, bevor das chemische Gleichgewicht erreicht ist.
- ⚖️ Die Gleichgewichtskonstante KC beschreibt das Verhältnis der Konzentrationen, wenn das chemische Gleichgewicht bereits erreicht ist.
- 🔄 Wenn QC kleiner als KC ist, läuft die Netto-Reaktion von links nach rechts, das heißt, die Konzentration der Produkte nimmt zu.
- ⬇️ Wenn QC größer als KC ist, läuft die Netto-Reaktion von rechts nach links, die Konzentration der Edukte nimmt zu.
- 🧪 QC wird genauso wie KC nach dem Massenwirkungsgesetz berechnet, der Unterschied besteht darin, dass QC den aktuellen Zustand der Reaktion zeigt.
- 🍴 Das Beispiel mit den Esslöffeln verdeutlicht die Netto-Reaktionsrichtung: Entstehen mehr Produkte als verbraucht werden, steigt die Konzentration der Produkte.
- ⏳ Die Netto-Reaktionsrichtung gibt an, wie sich die Konzentrationen von Produkten und Edukten verändern, bevor das chemische Gleichgewicht erreicht ist.
- 🔄 Die Netto-Reaktionsrichtung unterscheidet sich von der Hin- und Rückreaktion, sie bezieht sich auf die Gesamtkonzentration von Produkten und Edukten.
- 📉 QC wird kleiner, wenn die Konzentration der Edukte hoch ist, und größer, wenn die Konzentration der Produkte steigt.
- 📈 Das Ziel ist es, dass der QC-Wert sich dem KC-Wert angleicht. Wenn beide gleich sind, ist das chemische Gleichgewicht erreicht.
Q & A
Was ist der Reaktionsquotient (Qc) und wie unterscheidet er sich von der Gleichgewichtskonstanten (Kc)?
-Der Reaktionsquotient (Qc) beschreibt das Verhältnis der Konzentrationen von Produkten und Edukten zu einem bestimmten Zeitpunkt, wenn das chemische Gleichgewicht noch nicht erreicht ist. Im Gegensatz dazu beschreibt die Gleichgewichtskonstante (Kc) das Verhältnis im chemischen Gleichgewicht.
Wie erkennt man anhand von Qc und Kc, in welche Richtung die Reaktion abläuft?
-Wenn Qc kleiner als Kc ist, läuft die Reaktion von links nach rechts (Hinreaktion), und die Konzentration der Produkte nimmt zu. Ist Qc größer als Kc, läuft die Reaktion von rechts nach links (Rückreaktion), und die Edukte nehmen zu.
Was bedeutet die Netto-Reaktionsrichtung?
-Die Netto-Reaktionsrichtung beschreibt, ob die Konzentration der Produkte oder Edukte insgesamt zunimmt. Wenn die Netto-Reaktion nach rechts verläuft, entstehen mehr Produkte. Läuft sie nach links, entstehen mehr Edukte.
Wie berechnet man den Reaktionsquotienten Qc?
-Qc wird berechnet, indem man das Verhältnis der Konzentrationen der Produkte zu den Edukten nimmt, wobei die Konzentrationen der Produkte im Zähler und die der Edukte im Nenner stehen. Die Exponenten entsprechen den Koeffizienten der Reaktionsgleichung.
Was passiert, wenn Qc gleich Kc ist?
-Wenn Qc gleich Kc ist, befindet sich das System im chemischen Gleichgewicht, und es gibt keine Netto-Veränderung der Konzentrationen von Produkten und Edukten.
Warum ist es wichtig, zwischen der Netto-Reaktion und den Hin- und Rückreaktionen zu unterscheiden?
-Die Netto-Reaktion gibt die allgemeine Veränderung der Konzentrationen an, während Hin- und Rückreaktionen parallel stattfinden. Die Netto-Reaktion beschreibt, welche Reaktion stärker ist und somit die Richtung der Gesamtveränderung bestimmt.
Welche Rolle spielt die Stoffmenge bei der Berechnung von Qc?
-In manchen Fällen, wenn die Koeffizienten der Reaktionsgleichung auf beiden Seiten gleich sind, kann man die Stoffmenge (in Mol) anstelle der Konzentration verwenden, um Qc zu berechnen.
Wie beeinflusst eine hohe Eduktkonzentration den Qc-Wert?
-Eine hohe Konzentration der Edukte führt zu einem niedrigen Qc-Wert, da die Edukte im Nenner des Bruchs stehen.
Wie kann man die Richtung der Reaktion für ein bestimmtes Beispiel feststellen?
-Indem man Qc für die gegebenen Stoffmengen berechnet und ihn mit dem Kc-Wert vergleicht, kann man die Richtung der Reaktion bestimmen. Wenn Qc kleiner ist als Kc, verläuft die Reaktion nach rechts (Produktbildung).
Was bedeutet es, wenn die Netto-Reaktionsrichtung nach rechts verläuft?
-Wenn die Netto-Reaktionsrichtung nach rechts verläuft, werden mehr Produkte als Edukte gebildet, und die Konzentration der Produkte nimmt zu.
Outlines

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифMindmap

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифKeywords

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифHighlights

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифTranscripts

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифПосмотреть больше похожих видео

Schutzmaßnahme Nullung - Die Grundlagen

Hypertonisch - Hypotonisch - Isotonisch [Konzentrationen von Lösungen + Klausurtipp] - [Biologie]

Unser Tubulussystem erklärt (Wie wird aus Blut, Urin) Teil 1

Periodensystem der Elemente I Teil 2 I musstewissen Chemie
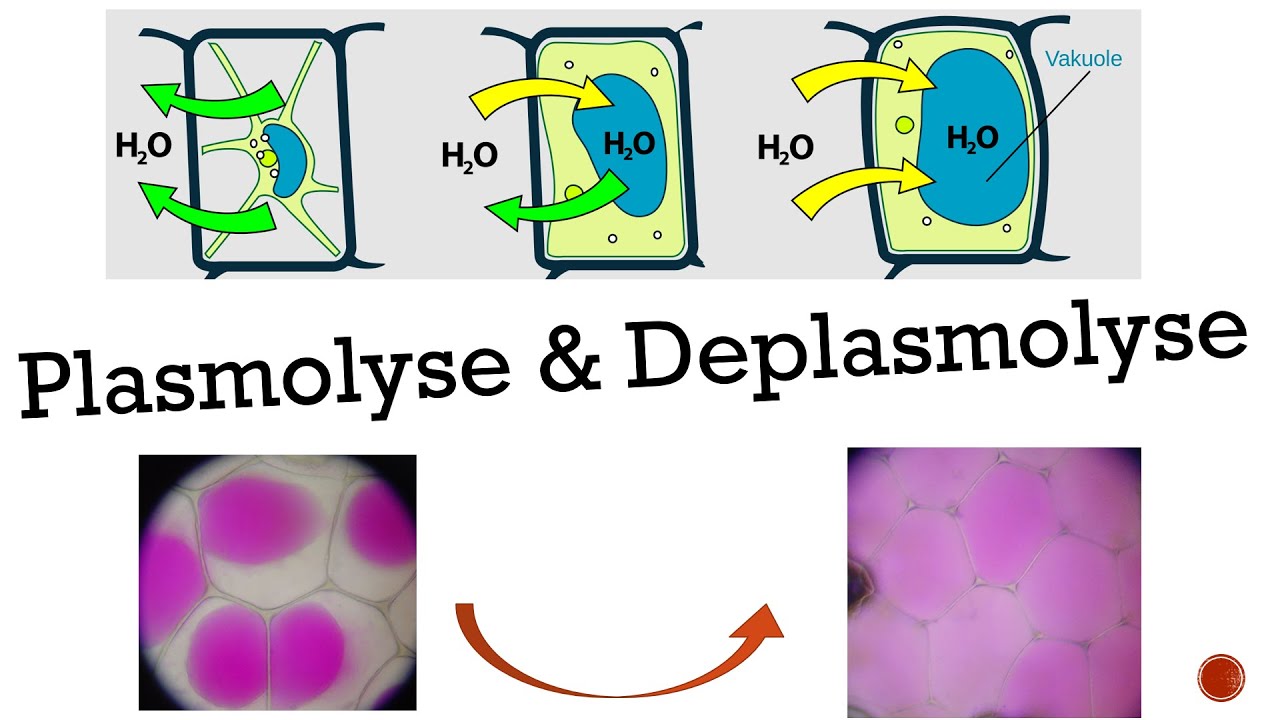
Plasmolyse & Deplasmolyse [Biologie, Oberstufe]

Was ist dem Vorwurf, die Nürnberger Prozesse seien "Siegerjustiz" gewesen, zu entgegnen?
5.0 / 5 (0 votes)
