[SANGAT MUDAH] Cara menghitung kalor reaksi pada kalorimeter (PART 2)
Summary
TLDRIn this educational video, the host discusses how to calculate the enthalpy of combustion using a calorimeter. The first problem involves the combustion of 8 grams of methane, resulting in a temperature rise from 25.5°C to 95°C in a 4-liter water calorimeter. Using the heat capacity of water and assuming the calorimeter's capacity is zero, the enthalpy of combustion is calculated to be -2184 kJ/mol. The second problem examines a reaction between nickel and CuSO4 solution, causing a 5°C temperature increase. The reaction's enthalpy is determined to be -4000 kJ/mol under standard conditions, showcasing the application of thermodynamics in chemical reactions.
Takeaways
- 🔍 The video discusses how to calculate the enthalpy change using a calorimeter.
- 🔥 The first problem involves the combustion of 8 grams of methane, resulting in a temperature rise in the calorimeter.
- 🌡️ The calorimeter's temperature increases from 25.5°C to 95°C due to the reaction.
- 💧 The calorimeter contains 4 liters of water, and the specific heat capacity of water is given as 4.2 J/g°C.
- ⚖️ The mass of the water in the calorimeter is calculated to be 4000 grams, assuming 1 liter is equivalent to 1 kilogram.
- 🔢 The change in temperature (ΔT) is calculated as the difference between the final and initial temperatures.
- 🔄 The enthalpy change of the reaction is calculated using the formula: \( \Delta H_{reaction} = -(mass_{water} \times c_{water} \times \Delta T) \).
- 🌐 The calorimeter's heat capacity is considered zero, simplifying the calculation.
- 🔄 The moles of methane burned are calculated by dividing the mass by the molar mass.
- 🔍 The final enthalpy change per mole of methane is determined by dividing the total enthalpy change by the moles of methane.
- 🧪 The second problem involves a reaction between nickel and a CuSO4 solution, causing a 5°C temperature increase in the solution.
Q & A
What is the mass of methane (CH4) burned in the first problem?
-The mass of methane (CH4) burned is 8 grams.
What is the initial and final temperature of the calorimeter in the first problem?
-The initial temperature is 25.5 degrees Celsius, and the final temperature is 95 degrees Celsius.
How much heat capacity does the calorimeter have in the first problem?
-The calorimeter is assumed to have a heat capacity of zero.
What is the heat capacity of water in the first problem?
-The heat capacity of water is 4.2 Joules per gram-degree Celsius.
How much heat is absorbed by the water in the first problem?
-The water absorbs 1092 kilojoules of heat.
What is the molar mass of methane (CH4) used in the first problem?
-The molar mass of methane (CH4) is 16 grams per mole.
What is the amount of methane (CH4) burned in moles in the first problem?
-Half a mole of methane (CH4) is burned.
What is the enthalpy change for the combustion of methane in kilojoules per mole in the first problem?
-The enthalpy change for the combustion of methane is -2184 kilojoules per mole.
What is the mass of nickel metal reacted with CuSO4 solution in the second problem?
-The mass of nickel metal reacted is 2.95 grams.
How much temperature increase is caused by the reaction of nickel metal with CuSO4 solution in the second problem?
-The reaction causes a 5-degree Celsius increase in the temperature of the solution.
What is the heat required to raise the temperature of the solution by 1 degree Celsius in the second problem?
-It requires 4 kilojoules of heat to raise the temperature of the solution by 1 degree Celsius.
What is the molar mass of nickel used in the second problem?
-The molar mass of nickel is 59 grams per mole.
How many moles of nickel are reacted in the second problem?
-0.05 moles of nickel are reacted.
What is the enthalpy change for the reaction of nickel with CuSO4 solution in kilojoules per mole in the second problem?
-The enthalpy change for the reaction is -40000 kilojoules per mole.
Outlines

This section is available to paid users only. Please upgrade to access this part.
Upgrade NowMindmap

This section is available to paid users only. Please upgrade to access this part.
Upgrade NowKeywords

This section is available to paid users only. Please upgrade to access this part.
Upgrade NowHighlights

This section is available to paid users only. Please upgrade to access this part.
Upgrade NowTranscripts

This section is available to paid users only. Please upgrade to access this part.
Upgrade NowBrowse More Related Video
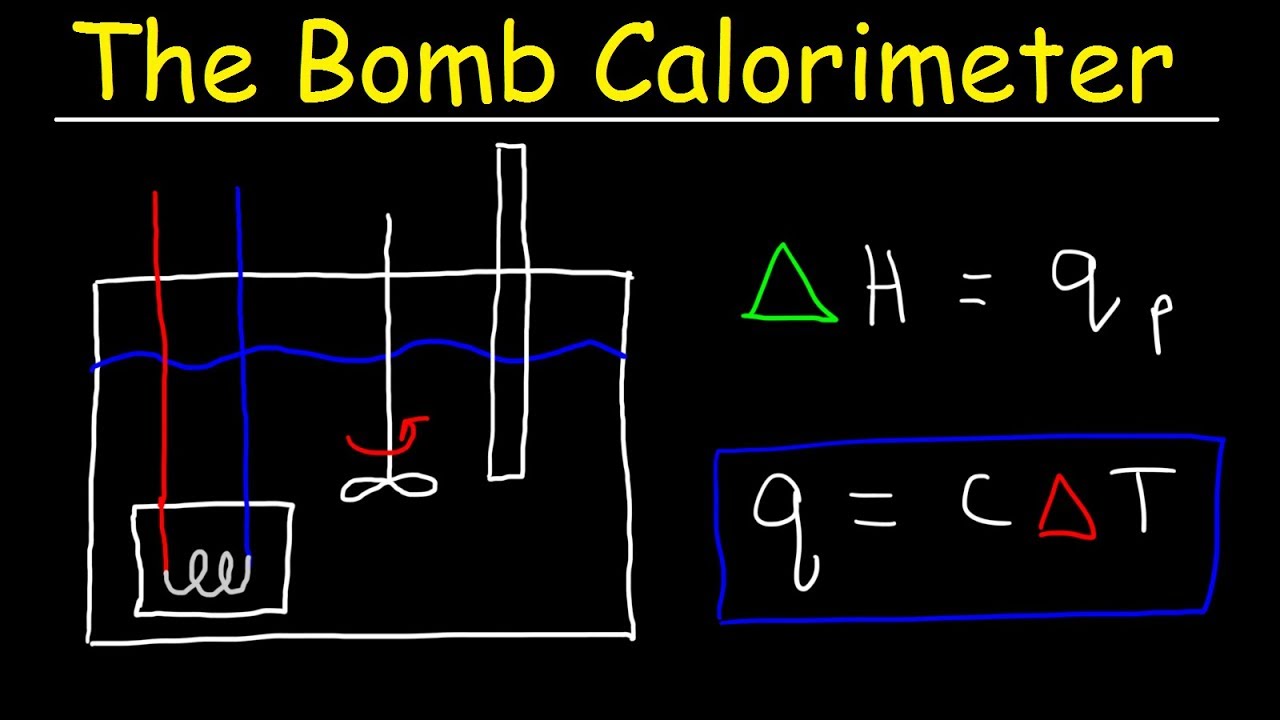
Bomb Calorimeter vs Coffee Cup Calorimeter Problem - Constant Pressure vs Constant Volume Calorimet

HUKUM HESS, ENTALPI PEMBENTUKAN DAN ENERGI IKATAN

KALORIMETER : Menghitung Perubahan Entalpi dengan Kalorimetri - Kimia kelas XI

Hukum Hess dengan Data Perubahan Entalpi Pembentukan Standar - Swasti
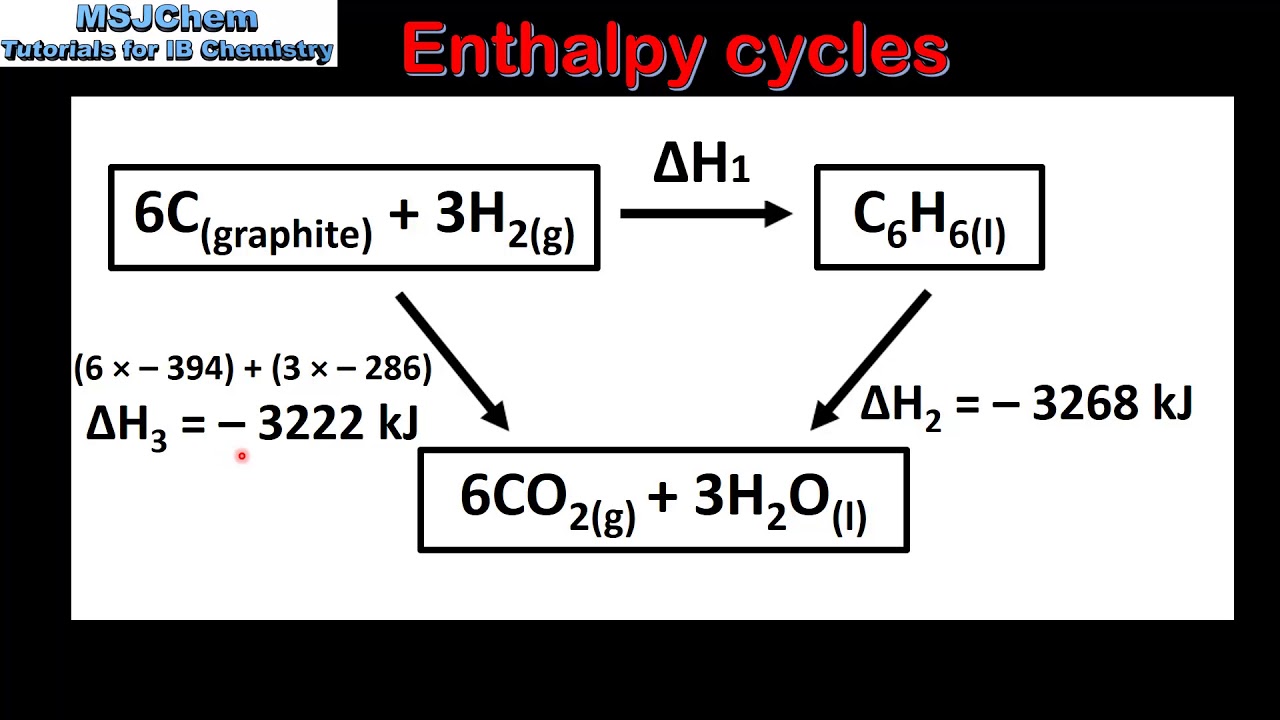
5.2 Enthalpy cycles (SL)

16.1 Thermochemistry
5.0 / 5 (0 votes)