PREPARASI LARUTAN INDUK, LARUTAN STANDAR & SAMPEL
Summary
TLDRThis educational video script focuses on teaching students the preparation of solutions needed for spectrophotometry analysis. It covers the creation of stock solutions, standard solutions, and samples, emphasizing the importance of understanding the difference between them. The script guides through the process of calculating the amount of substance required for solution preparation, weighing the solid materials, dissolving them, and diluting to the desired volume. It also explains how to prepare standard and blank solutions, and the requirements for samples in UV-Vis spectrophotometry, including the need for samples to be in solution form and to have color. The lesson concludes with a practical assignment for students to prepare a stock solution and a standard solution for an iron analysis experiment.
Takeaways
- 🔬 The lesson focuses on preparing solutions needed for spectrophotometry analysis.
- 📚 The main learning objectives include calculating the amount of materials required to make stock solutions, standard solutions, and understanding sample preparation.
- 🧪 Three types of solutions are discussed: stock solution, standard solution, and sample (analyte) solution.
- 📏 The stock solution is prepared from pure substances and is used to create standard solutions.
- 🔍 The procedure for preparing a stock solution involves weighing the solid substance, dissolving it in a solvent, and transferring it quantitatively into a volumetric flask.
- 🔢 Calculation of the amount of substance needed for a stock solution is demonstrated using the formula: mass of solute (g) = (concentration of stock solution (g/L) × volume of stock solution (L)) / 1000.
- 🌡 The preparation of a standard solution involves diluting the stock solution to a known concentration, using the dilution formula: M1V1 = M2V2, where M1 and V1 are the concentration and volume of the stock solution, and M2 and V2 are the desired concentration and volume of the standard solution.
- 🏼 The blank solution is prepared similarly to the standard solution but without the addition of the stock solution, to serve as a control.
- 🌈 For spectrophotometry, samples must be in solution form and should ideally be colored. If not, they can be oxidized or complexed to produce color.
- 📝 The students are tasked with designing a procedure to prepare a 1000 PPM stock solution and a 20 PPM standard solution for an analysis of iron content in river water.
Q & A
What is the main goal of the learning session described in the transcript?
-The main goal of the learning session is for the students to be able to calculate the amount of materials needed to prepare stock solutions, standard solutions, and sample solutions for spectrophotometry analysis.
What are the three types of solutions mentioned in the script that are needed for spectrophotometry analysis?
-The three types of solutions mentioned are stock solution, standard solution, and sample solution.
What is a stock solution and how is it prepared?
-A stock solution is a solution made from a pure solid substance that will be diluted to create several standard solutions. It is prepared by weighing the solid substance, dissolving it in a solvent, and then quantitatively transferring it into a volumetric flask to make up to the mark with the solvent.
How is the amount of substance needed for making a stock solution calculated?
-The amount of substance needed for making a stock solution is calculated using the formula: mass of solute (g) = (concentration of stock solution (g/L) × volume of stock solution (L)) / 1000.
What is a standard solution and how is it different from a stock solution?
-A standard solution is a solution with a known and precise concentration of the analyte, prepared from the stock solution by dilution. It is different from a stock solution in that it has a lower concentration and is used for calibration or to prepare other solutions with specific concentrations.
What is the purpose of a blank solution in spectrophotometry?
-A blank solution in spectrophotometry is a solution that receives the same treatment as the sample but does not contain the analyte of interest. It is used to account for any background absorbance or interferences that may affect the measurements.
Why must samples be in solution form for UV-Vis spectrophotometry?
-Samples must be in solution form for UV-Vis spectrophotometry because the technique measures the absorbance of light by the sample, which can only be accurately done when the sample is in a homogeneous solution.
What are the two methods mentioned in the script to make colorless samples colored for spectrophotometry?
-The two methods mentioned to make colorless samples colored are oxidation to form colored ions, such as converting colorless Mn to pink permanganate ions, and the formation of colored complexes by adding complexing agents, such as turning colorless Fe ions into red complexes with thiocyanate.
What is the task given to the students at the end of the transcript?
-The task given to the students is to perform an evaluation exercise in their book, which involves preparing 100 ml of a 1000 ppm stock solution and 100 ml of a 20 ppm standard solution for the analysis of iron content in river water using a UV-Vis spectrophotometer.
What is the key message the instructor emphasizes for success in learning?
-The key message emphasized by the instructor for success in learning is the importance of action, as indicated by the phrase 'tindakan kalian tindakan untuk selalu belajar itu adalah kunci kalian untuk menuju kesuksesan', which translates to 'your actions, the actions to always learn, are the keys to your success'.
Outlines

Esta sección está disponible solo para usuarios con suscripción. Por favor, mejora tu plan para acceder a esta parte.
Mejorar ahoraMindmap

Esta sección está disponible solo para usuarios con suscripción. Por favor, mejora tu plan para acceder a esta parte.
Mejorar ahoraKeywords

Esta sección está disponible solo para usuarios con suscripción. Por favor, mejora tu plan para acceder a esta parte.
Mejorar ahoraHighlights

Esta sección está disponible solo para usuarios con suscripción. Por favor, mejora tu plan para acceder a esta parte.
Mejorar ahoraTranscripts

Esta sección está disponible solo para usuarios con suscripción. Por favor, mejora tu plan para acceder a esta parte.
Mejorar ahoraVer Más Videos Relacionados

Penentuan Kadar Miconazole dalam salep dengan menggunakan metode Spektrofotometri Uv-Vis

materi seni budaya kelas 9 / bernyanyi lagu modern
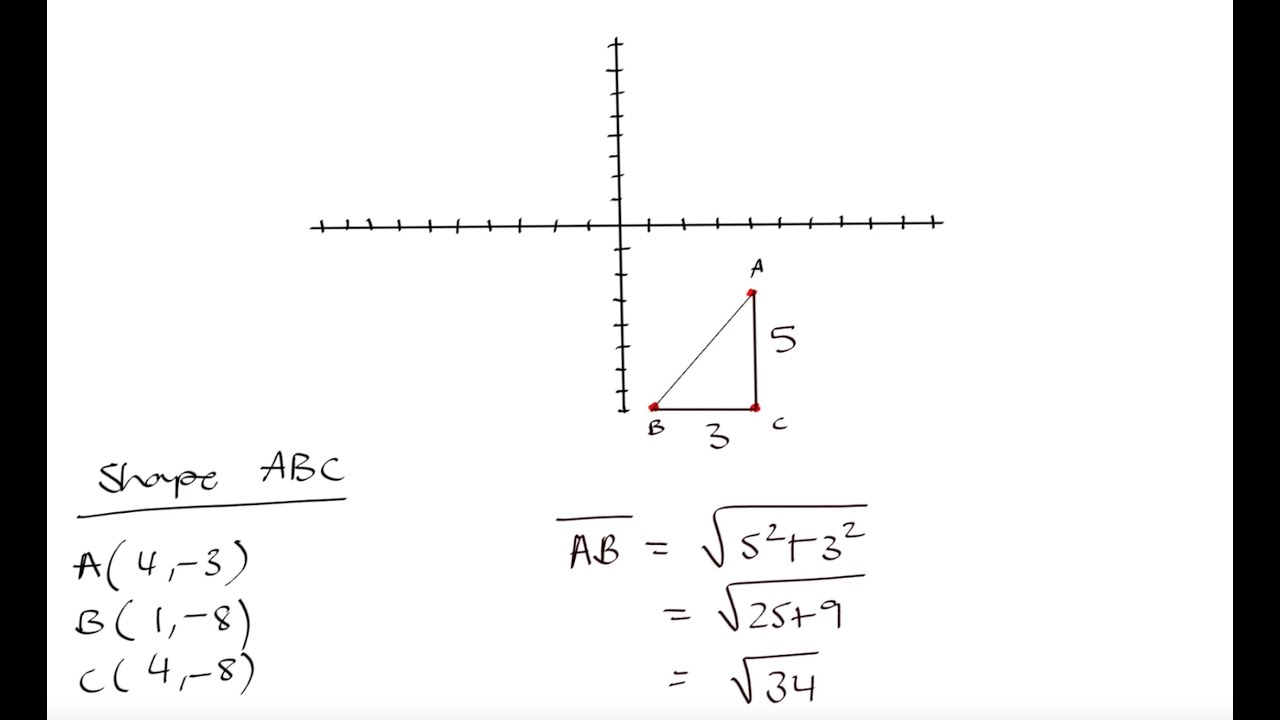
Grade 10 Math: Drawing geometric figures on a Cartesian plane

Pemantapan Kemampuan Mengajar

Pembahasan Laboratory Case B3 : Spektrofotometer

PERMASALAHAN GURU DAN SOLUSINYA
5.0 / 5 (0 votes)
