Fisika Atom • Part 2: Teori Atom Bohr
Summary
TLDRفي هذا الفيديو، يتم شرح نظرية الذرة لبور التي قدمها نيلز بور في عام 1913. يتم التطرق إلى نموذج الذرة الذي يشمل مسارات الإلكترونات الثابتة التي لا تشع أو تمتص الطاقة أثناء دورانها. يتم شرح القوانين المتعلقة بالمسارات والإلكترونات، وكيفية امتصاص أو انبعاث الطاقة. كما يتم استعراض المعادلات الرياضية لحساب نصف قطر ومسافة الإلكترون في المدارات المختلفة والطاقة الإجمالية للإلكترونات. في النهاية، يتم شرح العيوب في نموذج بور وتقديم نموذج ميكانيكا الكم كحل لهذه المشكلات.
Takeaways
- 😀 تم اقتراح نموذج الذرة لبور من قبل نيلز بور في عام 1913.
- 😀 في نموذج بور، تدور الإلكترونات في مدارات ثابتة حول النواة دون إصدار أو امتصاص للطاقة.
- 😀 كل مدار إلكتروني له مستوى طاقة معين، ويمكن أن يتم امتصاص أو إصدار الطاقة عندما ينتقل الإلكترون بين هذه المدارات.
- 😀 المسار الإلكترون في المدارات يحدد حسب رقم الكم الرئيسي (n)، وكلما كانت المدارات أبعد عن النواة، زادت طاقتها.
- 😀 المعادلة لحساب نصف قطر المدار الإلكتروني هي: r_n = n^2 × r1، حيث أن r1 = 5.3 × 10^-11 متر.
- 😀 المعادلة لحساب الطاقة الإجمالية للإلكترون هي: E_n = -13.6 / n^2 إلكترون فولت.
- 😀 نموذج بور يشرح بشكل جيد الذرة الهيدروجينية ولكنه غير قادر على تفسير الذرات متعددة الإلكترونات.
- 😀 في نموذج بور، الإلكترونات لا تُشع طاقة أثناء دورانها في المدارات الثابتة.
- 😀 نموذج بور يمكنه شرح الطيف الذري للهيدروجين فقط، ولا يمكن تطبيقه على الذرات التي تحتوي على أكثر من إلكترون.
- 😀 لتحديد نصف قطر وطاقة المدار الرابع (n=4) في ذرة الهيدروجين، يتم استخدام المعادلات المذكورة للحصول على نصف القطر 8.8 × 10^-10 متر والطاقة -0.85 إلكترون فولت.
- 😀 تم تحسين نموذج بور باستخدام ميكانيكا الكم، خاصة بواسطة إروين شرودنغر.
Q & A
ما هو نموذج الذرة الذي قدمه نيلز بور في عام 1913؟
-نموذج الذرة الذي قدمه نيلز بور في عام 1913 هو نموذج يعتمد على وجود مسارات محددة للإلكترونات حول النواة. يتميز هذا النموذج بأن الإلكترونات لا تشع أو تمتص الطاقة أثناء تحركها في المسارات الثابتة.
ما هي الافتراضات الرئيسية لنموذج بور؟
-الافتراضات الرئيسية لنموذج بور هي: 1) الإلكترونات تتحرك في مدارات ثابتة حول النواة دون أن تشع أو تمتص طاقة. 2) الإلكترونات تمتص أو تشع طاقة عندما تنتقل من مدار إلى آخر.
ما هو معنى مستوى الطاقة في سياق نموذج بور؟
-مستوى الطاقة في نموذج بور يمثل الطبقات أو المدارات التي يمكن أن توجد فيها الإلكترونات. كل مدار يحتوي على طاقة محددة، وكلما كان المدار أبعد عن النواة، كانت الطاقة أعلى.
كيف يحدد نموذج بور الطاقة التي يمتصها أو يطلقها الإلكترون؟
-عندما ينتقل الإلكترون من مدار داخلي إلى مدار خارجي، يمتص طاقة مقدارها HF (حيث H هو ثابت بلانك وF هو تردد الفوتون). وعندما ينتقل الإلكترون من مدار خارجي إلى داخلي، يطلق طاقة مقدارها HF.
كيف يتم حساب نصف قطر مدار الإلكترون باستخدام نموذج بور؟
-نصف قطر مدار الإلكترون في نموذج بور يُحسب باستخدام الصيغة: Rn = n² * R1، حيث R1 هو نصف قطر المدار الأول (5.3 × 10⁻¹¹ متر) وn هو رقم المدار (1، 2، 3، ...).
ما هي العلاقة بين الطاقة في مدار معين ونصف قطره في نموذج بور؟
-الطاقة في مدار معين تُحسب باستخدام الصيغة: En = -13.6 / n² إلكترون فولت، حيث n هو رقم المدار. كلما زاد n، انخفضت الطاقة.
ما هي عيوب نموذج بور؟
-عيوب نموذج بور تشمل: 1) المدار الإلكتروني ليس بالضرورة دائريًا، بل معقد. 2) النموذج لا يمكنه تفسير الذرات متعددة الإلكترونات بشكل دقيق. 3) لا يفسر تأثير الحقول المغناطيسية على طيف الذرة. 4) لا يفسر بشكل جيد التفاعلات الكيميائية.
كيف تختلف المدارات في نموذج بور عن نموذج رذرفورد؟
-في نموذج رذرفورد، كان يُعتقد أن الإلكترونات تتحرك بشكل عشوائي حول النواة، بينما في نموذج بور، المدارات ثابتة ولها قيم محددة للطاقة، ولا تشع الإلكترونات طاقة أثناء تحركها في تلك المدارات.
كيف يمكن استخدام نموذج بور لحساب نصف قطر طيف الهيدروجين في مستوى معين؟
-لحساب نصف القطر في مستوى معين، نستخدم الصيغة: Rn = n² * R1، حيث n هو رقم المستوى، وR1 هو نصف القطر للمستوى الأول (5.3 × 10⁻¹¹ متر).
كيف يمكن حساب الطاقة الإجمالية للإلكترون في مستوى معين باستخدام نموذج بور؟
-لحساب الطاقة الإجمالية للإلكترون في مستوى معين، نستخدم الصيغة: En = -13.6 / n² إلكترون فولت، حيث n هو رقم المدار. على سبيل المثال، للطاقة في المدار الرابع (n=4)، تكون En = -13.6 / 16 = -0.85 إلكترون فولت.
Outlines

此内容仅限付费用户访问。 请升级后访问。
立即升级Mindmap

此内容仅限付费用户访问。 请升级后访问。
立即升级Keywords

此内容仅限付费用户访问。 请升级后访问。
立即升级Highlights

此内容仅限付费用户访问。 请升级后访问。
立即升级Transcripts

此内容仅限付费用户访问。 请升级后访问。
立即升级浏览更多相关视频

Teori Relativitas Khusus | Fisika SMA

Why Does Popcorn Pop? | The Science of Food! | SciShow Kids
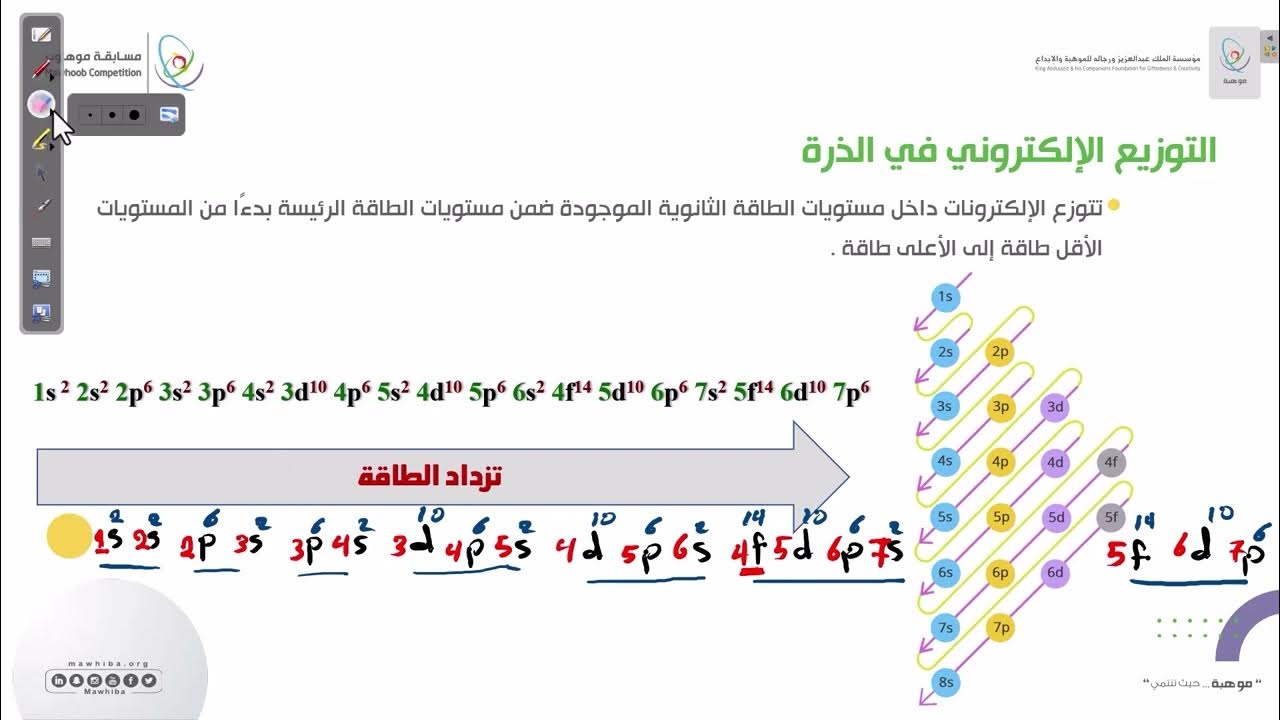
مسابقة موهوب 2 - (الكيمياء): التوزيع الإلكتروني في الذرة 2

محاضرة 4 | الدرس 6 | Changes in interface in Java 8 and 9

Sc Edu U5 Seq3

Perbedaan Whitebox, Blackbox dan Graybox Testing pada perangkat lunak

Sc Ed U5 Seq4
5.0 / 5 (0 votes)
