Conjugation & UV-Vis Spectroscopy: Crash Course Organic Chemistry #41
Summary
TLDRIn diesem Crash Course Organic Chemistry-Video erklärt Deboki Chakravarti, wie konjugierte Elektronensysteme die Stabilität von Molekülen beeinflussen. Anhand des Beispiels von Beta-Carotin und Goldenem Reis wird veranschaulicht, wie Vitamin A Mangelkrankheiten wie Nachtblindheit verursacht und durch gentechnisch veränderte Nahrungsmittel bekämpft werden kann. Das Video taucht in die Physik von kovalenten Bindungen ein, beleuchtet die Rolle von Molekülorbitalen und UV-Spektroskopie und erklärt, wie konjugierte Moleküle Licht absorbieren, wodurch ihre Farben sichtbar werden. Ein spannender Einblick in die Bedeutung organischer Chemie für Gesundheit und Alltag.
Takeaways
- 🥕 Vitamin A ist essentiell für die Gesundheit und kann über Lebensmittel wie Fleisch, Fisch, Eier und Milchprodukte aufgenommen werden.
- 🌾 Goldenes Reis wurde gentechnisch verändert, um Beta-Carotin zu produzieren, das ein Vorläufer von Vitamin A ist.
- 🧪 Beta-Carotin ist ein Molekül mit einem konjugierten Elektronensystem, das ihm seine orange Farbe verleiht.
- 🌀 Konjugierte Alkene sind stabiler durch die Überlappung von Pi-Bindungen und Resonanzstrukturen.
- 💡 Konjugation stabilisiert Moleküle, was experimentell durch Enthalpieänderungen bei der Hydrierung gezeigt wird.
- 🔬 UV-Spektroskopie kann verwendet werden, um die Konzentration von konjugierten Molekülen wie Beta-Carotin zu messen.
- 🔵 Beta-Carotin absorbiert blaues Licht und erscheint deshalb orange.
- 👁 Vitamin A spielt eine Schlüsselrolle bei der Sehkraft, insbesondere bei der Umwandlung von Licht in elektrische Signale in den Augen.
- 🧬 Pi-Molekülorbitale entstehen, wenn p-Atomorbitale überlappen, was zu verschiedenen Energieniveaus führt.
- 📏 Die UV-Spektroskopie hilft, den Konzentrationsgrad eines Moleküls durch Messung der absorbierten Lichtmenge zu bestimmen.
Q & A
Was ist ein Beispiel für eine organische Verbindung, die unser Körper benötigt, aber nicht selbst herstellen kann?
-Vitamin A ist ein Beispiel für eine organische Verbindung, die unser Körper benötigt, aber nicht selbst herstellen kann.
Wie wird der Vitamin-A-Mangel in einigen Regionen der Welt bekämpft?
-Eine Lösung ist die Einführung von 'Goldenem Reis', einer gentechnisch veränderten Reissorte, die Beta-Carotin produziert, das ein Vorläufer von Vitamin A ist.
Warum erscheint Beta-Carotin orange?
-Beta-Carotin erscheint orange, weil es durch sein konjugiertes Elektronensystem blaues Licht absorbiert, während orangefarbenes Licht unser Auge erreicht.
Was bedeutet Konjugation in Bezug auf Moleküle?
-Konjugation bedeutet, dass ein Molekül alternierende Einzel- und Doppelbindungen hat, was die Stabilität des Moleküls erhöht.
Wie zeigt die Hydrierung von 1,3-Butadien, dass konjugierte Doppelbindungen ein Molekül stabilisieren?
-Die Hydrierung von 1,3-Butadien hat eine geringere Enthalpieänderung (-237 kJ/mol) als die von Penta-1,4-dien (-252 kJ/mol), was zeigt, dass konjugierte Doppelbindungen das Molekül stabilisieren.
Was ist eine kovalente Bindung?
-Eine kovalente Bindung ist, wenn zwei Atome ein Elektronenpaar teilen. Diese Bindung entsteht durch das Gleichgewicht von anziehenden und abstoßenden Kräften zwischen Elektronen und Atomkernen.
Was ist der Unterschied zwischen einem bindenden und einem antibindenden Orbital?
-Ein bindendes Orbital entsteht, wenn die Phasen der p-Orbitale übereinstimmen und die Anziehungskräfte überwiegen, während ein antibindendes Orbital entsteht, wenn die Phasen entgegengesetzt sind und die Abstoßungskräfte dominieren.
Was ist UV-Spektroskopie und wie wird sie verwendet?
-UV-Spektroskopie misst, wie Moleküle UV-Licht absorbieren, um Informationen über ihre Struktur zu gewinnen, insbesondere über konjugierte Pi-Systeme. Sie kann zur Bestimmung der Konzentration von Molekülen wie Beta-Carotin verwendet werden.
Warum kann ein Vitamin-A-Mangel zu Nachtblindheit führen?
-Vitamin-A-Mangel kann zu Nachtblindheit führen, weil es ein wichtiger Bestandteil von 11-cis-Retinal ist, das in Rhodopsin umgewandelt wird, einem lichtempfindlichen Molekül in den Stäbchenzellen des Auges.
Was passiert, wenn Butadien UV-Licht ausgesetzt wird?
-Wenn Butadien UV-Licht ausgesetzt wird, absorbiert es die Energie, was dazu führt, dass Elektronen vom HOMO in das LUMO springen, was als Pi-Pi-Stern-Anregung bezeichnet wird.
Outlines

此内容仅限付费用户访问。 请升级后访问。
立即升级Mindmap

此内容仅限付费用户访问。 请升级后访问。
立即升级Keywords

此内容仅限付费用户访问。 请升级后访问。
立即升级Highlights

此内容仅限付费用户访问。 请升级后访问。
立即升级Transcripts

此内容仅限付费用户访问。 请升级后访问。
立即升级浏览更多相关视频

Dipole und ihre Wechselwirkungen
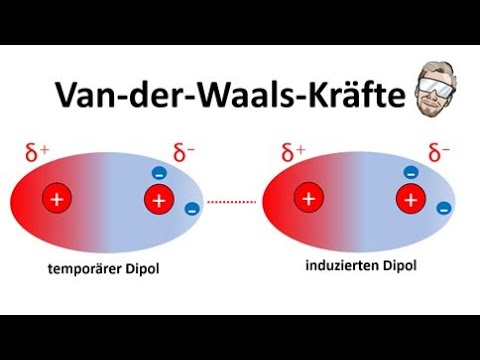
Van der Waals Kräfte | Einfluss auf die Siedetemperatur | Chemie Endlich Verstehen

Carboxylic Acids: Crash Course Organic Chemistry #30

Crash Course Organic Chemistry Preview
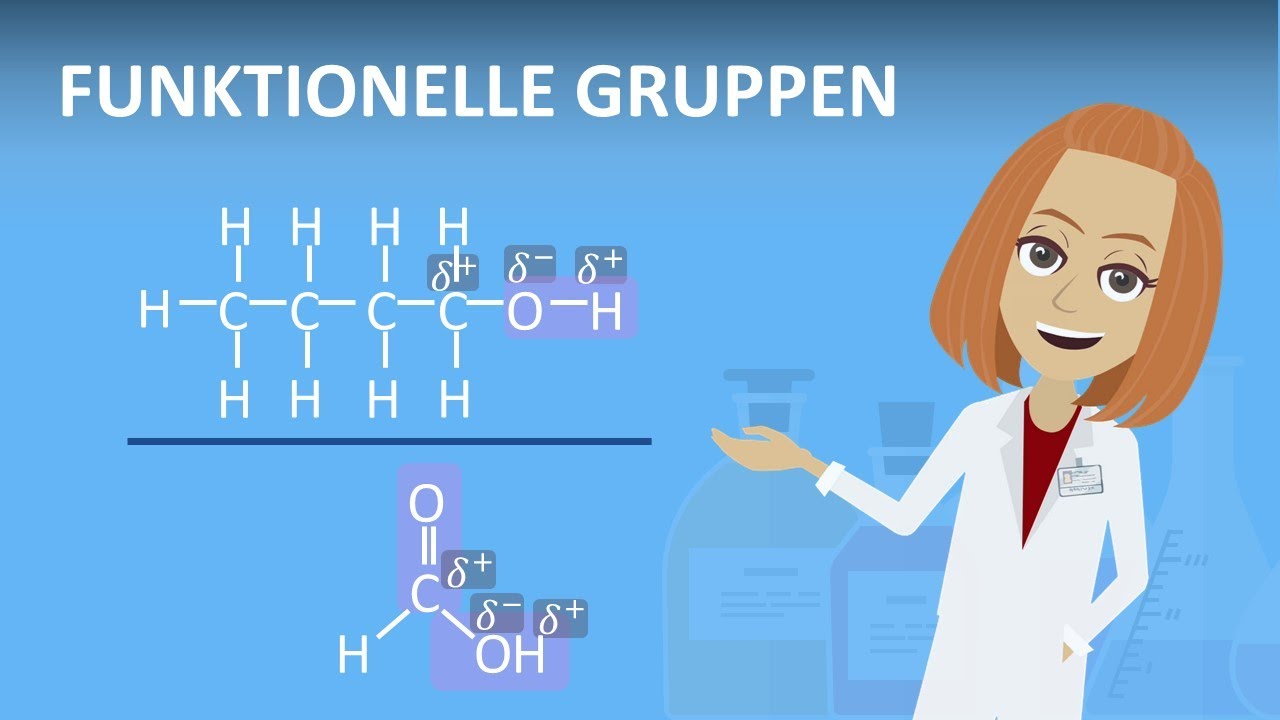
Funktionelle Gruppen - Übersicht, Tabelle & Erklärung | Studyflix

Einfach erklärt: London-Disperions- Dipol-Dipol- H-Brücken-Wechselwirkungen 4k 60Fps
5.0 / 5 (0 votes)
