Fórmula Mínima y Molecular | Química | Materia y sus Propiedades | Video 12 | Egg Educación
Summary
TLDREn este video, se enseña cómo determinar la fórmula mínima y la fórmula molecular de un compuesto. Se presenta un ejemplo con 10 gramos de un compuesto de carbono, hidrógeno y oxígeno con un peso molecular de 60 gramos por mol. El procedimiento incluye calcular porcentajes de los elementos, dividir por sus pesos moleculares, normalizar los resultados y determinar la fórmula mínima. Luego, se calcula un valor 'n' basado en el cociente entre el peso molecular del compuesto y la fórmula mínima, para finalmente obtener la fórmula molecular. El video enfatiza la importancia de trabajar con números enteros y proporciona estrategias para manejar decimales en los cálculos.
Takeaways
- 🎵 Hola chicos, en este vídeo aprenderemos a determinar la fórmula mínima y la fórmula molecular de un compuesto.
- 🔬 Este tipo de ejercicios involucra una muestra de masa conocida con un peso molecular determinado y diferentes átomos.
- 🧪 El primer paso es transformar las masas de los átomos en porcentajes.
- 📊 Ejemplo: 4 gramos de carbono es el 40% de una muestra de 10 gramos; 0.67 gramos de hidrógeno es el 6.7% y 5.33 gramos de oxígeno es el 53.3%.
- ⚖️ El segundo paso es dividir cada porcentaje por el peso molecular correspondiente: carbono (12), hidrógeno (1), oxígeno (16).
- ➗ Después, dividimos cada resultado por el número más pequeño obtenido entre ellos.
- 📏 Si los números no son enteros, hay que multiplicar todos los resultados por un factor para obtener enteros.
- 📄 La fórmula mínima se determina con los números enteros resultantes.
- 🧮 Para obtener la fórmula molecular, calculamos un valor n basado en el cociente del peso molecular dado y el peso molecular de la fórmula mínima.
- 📚 El ejercicio es mecánico, así que se recomienda practicar varios ejemplos para dominar el proceso.
Q & A
¿Qué se va a aprender en el video?
-En el video se va a aprender a determinar la fórmula mínima y la fórmula molecular de un compuesto.
¿Cuál es el primer paso para determinar las fórmulas de un compuesto según el video?
-El primer paso es convertir las masas en porcentajes de los elementos presentes en la muestra.
¿Cómo se calcula el porcentaje de carbono en la muestra del ejemplo del video?
-Si la muestra pesa 10 gramos y el carbono tiene 4 gramos, el porcentaje de carbono es (4/10) * 100 = 40%.
¿Qué es el peso molecular y cómo se relaciona con el segundo paso del procedimiento?
-El peso molecular es la masa total de un mol de una sustancia. En el segundo paso, se dividen los porcentajes obtenidos por el peso molecular correspondiente de cada elemento.
¿Cuál es el peso molecular del hidrógeno y cómo se usa en el procedimiento?
-El peso molecular del hidrógeno es 1. Se divide el porcentaje de hidrógeno en la muestra por 1 para obtener una cantidad normalizada.
¿Qué significa el número más chico obtenido en el procedimiento y cómo se utiliza?
-El número más chico es el mínimo de los resultados obtenidos al dividir los porcentajes por los pesos moleculares. Se usa para normalizar los resultados dividiéndolos por este número.
¿Qué sucede si los resultados después de dividir por el número más chico no son enteros?
-Si los resultados no son enteros, se multiplica todo por 2 o por 3, dependiendo de los números, para que todos sean enteros y se pueda determinar la fórmula mínima.
¿Cómo se determina la fórmula mínima una vez que se tienen los números normalizados?
-Se toma el resultado normalizado de cada elemento y se interpreta como el número de átomos de ese elemento en la fórmula mínima.
¿Qué es el valor 'n' que se menciona en el video y cómo se calcula?
-El valor 'n' es el cociente del peso molecular anunciado por el peso molecular de la fórmula mínima. Se usa para determinar la fórmula molecular.
¿Cómo se calcula la fórmula molecular a partir de la fórmula mínima y el valor 'n'?
-Se multiplica cada número de la fórmula mínima por el valor 'n' para obtener los átomos en la fórmula molecular.
¿Por qué es importante realizar varios ejemplos según el video?
-Realizar varios ejemplos ayuda a familiarizarse con el procedimiento mecánico y a comprender mejor cómo determinar las fórmulas mínimas y moleculares.
Outlines

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифMindmap

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифKeywords

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифHighlights

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифTranscripts

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифПосмотреть больше похожих видео

Como obtener la fórmula empírica y molecular de un compuesto

Concepto de Fórmula Empírica y Fórmula Molecular
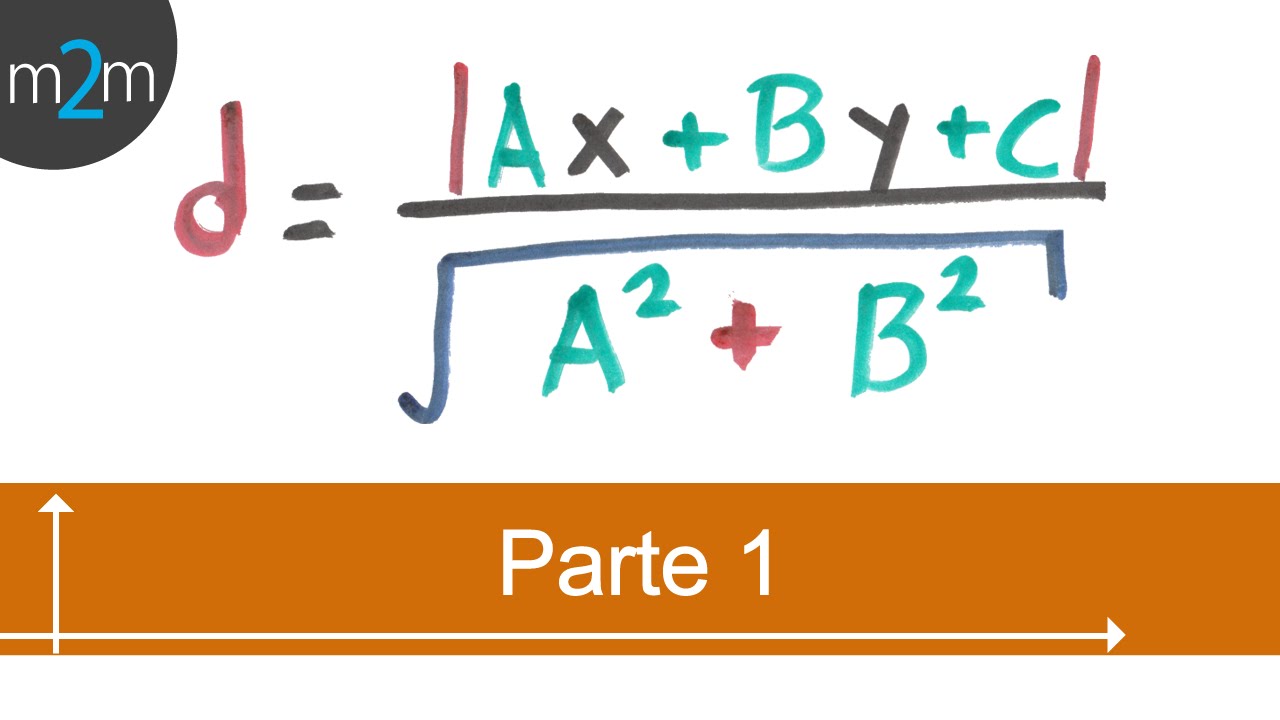
* Distancia entre un punto y una recta (PARTE 1)

FORMULA EMPIRICA Y MOLECULAR- COMPOSICIÓN PORCENTUAL | Acido facil

37. What is the equation of the line? FULL EXPLANATION

Estructuras de Lewis Ejemplo 2
5.0 / 5 (0 votes)
