Repaso Rápido de Propiedades Periódicas
Summary
TLDREl video aborda las propiedades periódicas de los elementos químicos, destacando cómo el carácter metálico aumenta hacia abajo y a la izquierda en la tabla periódica, mientras que las propiedades como el radio atómico y la electronegatividad varían en direcciones opuestas. Se explica que la energía de ionización aumenta hacia la derecha y hacia arriba, facilitando la formación de cationes. Finalmente, se menciona la afinidad electrónica y su relación con la formación de iones negativos, enfatizando la importancia de estas características en la predicción del comportamiento químico de los elementos.
Takeaways
- 😀 El carácter metálico de los elementos aumenta hacia abajo y hacia la izquierda de la tabla periódica.
- 😀 Los elementos metálicos son generalmente sólidos, duros y buenos conductores de electricidad y calor.
- 😀 Las propiedades periódicas son útiles para predecir el comportamiento químico de los elementos.
- 😀 El radio atómico aumenta hacia abajo y hacia la izquierda, lo que significa que los átomos son más grandes en esa dirección.
- 😀 La electronegatividad, que es la capacidad de atraer electrones, aumenta hacia arriba y hacia la derecha de la tabla periódica.
- 😀 Los no metales son más fuertes en atraer electrones en comparación con los metales.
- 😀 La energía de ionización es la energía necesaria para quitar un electrón de un átomo y aumenta hacia la derecha y hacia arriba.
- 😀 Los elementos en el extremo opuesto de la tabla se convierten fácilmente en cationes debido a su baja energía de ionización.
- 😀 La afinidad electrónica es la energía liberada cuando un átomo se une y aumenta hacia los no metales en la parte superior.
- 😀 Los no metales suelen formar iones negativos debido a su alta afinidad electrónica.
Q & A
¿Cómo se comportan los metales y no metales según la tabla periódica?
-El carácter metálico aumenta hacia abajo y hacia la izquierda de la tabla periódica, donde los elementos son sólidos duros que conducen bien la electricidad y el calor, mientras que los no metales se encuentran en el extremo opuesto y tienen propiedades contrarias.
¿Qué es el radio atómico y cómo varía en la tabla periódica?
-El radio atómico se refiere al tamaño de los átomos. Aumenta hacia abajo y hacia la izquierda en la tabla periódica, siendo los átomos más grandes los que se encuentran en estas posiciones.
¿Qué es la electronegatividad y cómo se comporta en la tabla periódica?
-La electronegatividad es la capacidad de un átomo para atraer electrones. Aumenta hacia arriba y hacia la derecha en la tabla periódica, lo que hace que los no metales sean más fuertes en la atracción de electrones.
¿Qué es la energía de ionización y cómo varía en la tabla periódica?
-La energía de ionización es la energía necesaria para quitarle un electrón a un átomo. Aumenta hacia la derecha y hacia arriba en la tabla periódica, haciendo que los elementos del extremo opuesto se conviertan fácilmente en cationes.
¿Qué significa que un elemento tenga alta afinidad electrónica?
-Una alta afinidad electrónica significa que el elemento puede convertirse en un ion con mayor facilidad, lo que generalmente se observa en los no metales que suelen formar iones negativos.
¿Por qué los no metales son fuertes en atraer electrones?
-Los no metales son fuertes en atraer electrones porque su electronegatividad es alta, lo que significa que tienen una mayor capacidad para atraer electrones hacia sí mismos.
¿Cómo se relacionan las propiedades periódicas con el comportamiento químico de los elementos?
-Las propiedades periódicas, como el radio atómico, la electronegatividad, la energía de ionización y la afinidad electrónica, son cruciales para predecir el comportamiento químico de los elementos.
¿Qué sucede con la energía de ionización en los metales?
-Los metales, ubicados en el extremo izquierdo de la tabla periódica, requieren poca energía para perder electrones, lo que los convierte en cationes con facilidad.
¿Qué es un catión?
-Un catión es un ion con carga positiva que se forma cuando un átomo pierde uno o más electrones.
¿Qué recursos adicionales se mencionan para aprender sobre el tema?
-Se menciona que se puede consultar el canal para obtener un tema más completo sobre las propiedades periódicas y el comportamiento químico de los elementos.
Outlines

このセクションは有料ユーザー限定です。 アクセスするには、アップグレードをお願いします。
今すぐアップグレードMindmap

このセクションは有料ユーザー限定です。 アクセスするには、アップグレードをお願いします。
今すぐアップグレードKeywords

このセクションは有料ユーザー限定です。 アクセスするには、アップグレードをお願いします。
今すぐアップグレードHighlights

このセクションは有料ユーザー限定です。 アクセスするには、アップグレードをお願いします。
今すぐアップグレードTranscripts

このセクションは有料ユーザー限定です。 アクセスするには、アップグレードをお願いします。
今すぐアップグレード関連動画をさらに表示
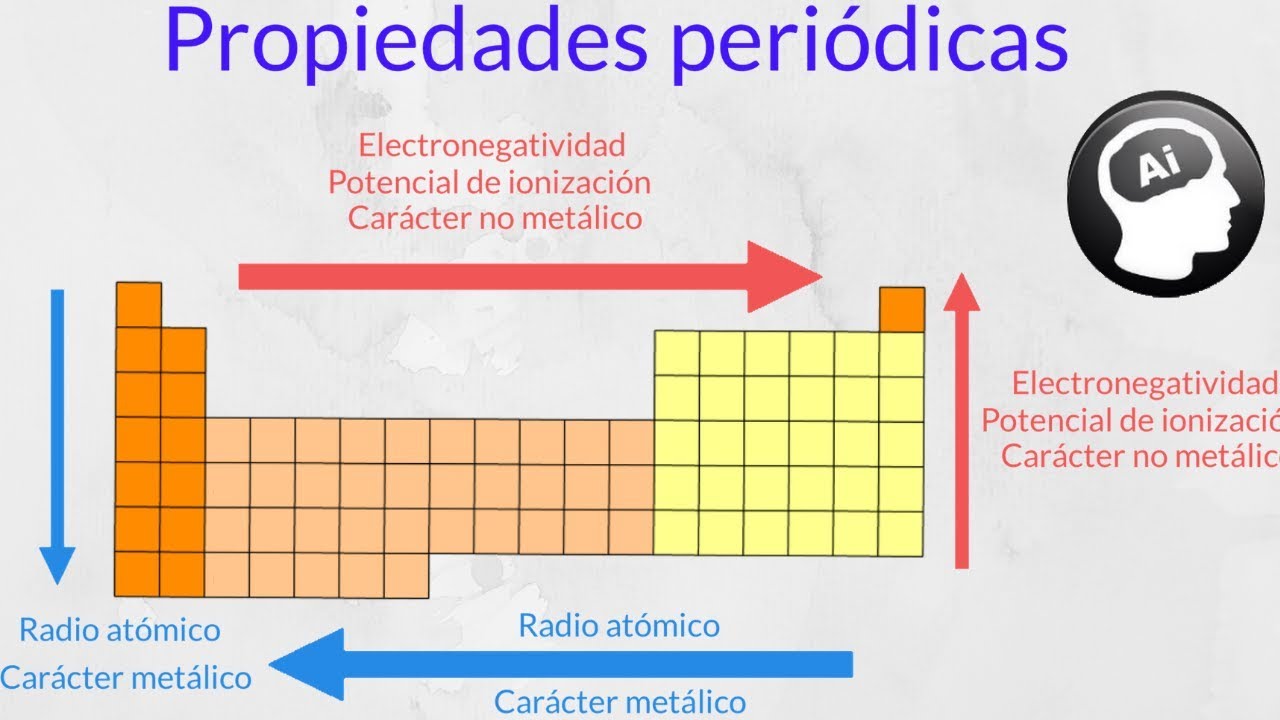
Como varían las propiedades periódicas de los elementos, electronegatividad, radio atomico

Las propiedades periódicas de los elementos

[Química] ✔ Propiedades periódicas 🔀 Tabla periódica.

Propiedades Periódicas de los Elementos. FÁCIL

PROPIEDADES PERIÓDICAS ► Aprende a ordenar los elementos ¡¡¡FACILÍSIMO!!!

💥 Propiedades Periódicas de los Elementos Químicos ⚗️ [Fácil y Rápido] | QUÍMICA |
5.0 / 5 (0 votes)
