CATABOLISMO DE AMINOÁCIDOS
Summary
TLDRIn this educational video, biochemist Karina Manuele explains the catabolism of amino acids, a crucial part of protein metabolism. She covers the breakdown of proteins into amino acids and their subsequent metabolic fates, including the formation of ammonia and carbon skeletons. The video delves into the importance of transamination reactions, facilitated by aminotransferases and vitamin B6, and their clinical significance as liver function markers.
Takeaways
- 😀 The video discusses amino acid catabolism, which is the breakdown of amino acids.
- 🌟 Amino acids are the building blocks of proteins and are broken down within our cells through proteolytic pathways.
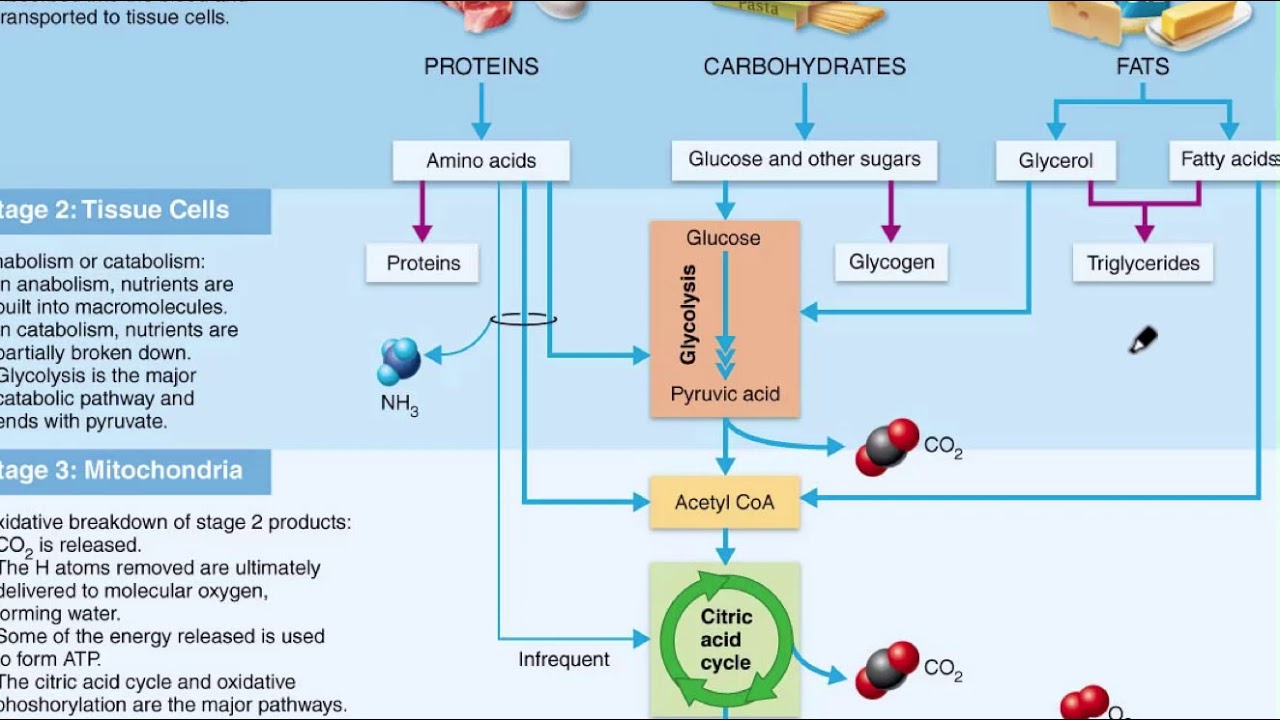
- 🔍 When amino acids are broken down, they are divided into an amino group (which becomes ammonium) and a carbon skeleton.
- ⚠️ Ammonium ions are toxic and must be quickly converted into urea in the liver or used in biosynthesis.
- 🌿 The carbon skeletons of amino acids can be converted into keto acids and may enter the citric acid cycle or be used for gluconeogenesis.
- 🧬 Transamination reactions are crucial for both the synthesis and degradation of amino acids.
- 🧪 The amino group from one amino acid is transferred to alpha-ketoglutarate by an enzyme called aminotransferase, forming glutamate and a keto acid.
- 🏥 Alanine aminotransferase (ALT) and aspartate aminotransferase (AST) are important enzymes used as liver function markers in clinical practice.
- 🍂 The video is part of a biochemistry course on YouTube aimed at helping viewers master biochemistry.
- 📈 The presenter, Karina Manuele, invites viewers to like, comment, subscribe, and support the channel for free educational content.
- 📚 The channel offers additional resources like summaries and mind maps to facilitate the study of metabolism.
Q & A
What is the main topic of the video?
-The main topic of the video is the catabolism of amino acids, which is the process of breaking down amino acids in our body.
Why is the catabolism of amino acids important?
-The catabolism of amino acids is important because it is a key pathway in protein metabolism. It allows for the breakdown of proteins into amino acids, which can then be used for various metabolic processes.
What happens to the amino acids after they are broken down?
-After amino acids are broken down, the amino group is released as an ammonium ion, and the remaining carbon chain becomes a carbon skeleton. These two parts have different fates in the body.
Why is the ammonium ion dangerous to the body?
-The ammonium ion is dangerous because it is neurotoxin and can easily cross the blood-brain barrier, causing harm. It needs to be quickly converted into a less harmful substance or used in biosynthesis.
What are the possible fates of the ammonium ion?
-The ammonium ion can either be used in biosynthetic pathways to form other amino acids or nucleotides, or it can be converted into urea in the liver through the urea cycle for safe excretion in urine.
What is the urea cycle and why is it important?
-The urea cycle is a series of biochemical reactions that occur in the liver and convert toxic ammonium ions into urea, which is then excreted in the urine. It is important for safely eliminating excess nitrogen from the body.
What are the carbon skeletons of amino acids used for?
-The carbon skeletons of amino acids can be converted into ketone bodies or undergo modifications to enter the TCA cycle for energy production or gluconeogenesis for glucose synthesis.
What is transamination and why is it important in amino acid metabolism?
-Transamination is a reaction where an amino group is transferred from an amino acid to an alpha-keto acid, forming a new amino acid and a new alpha-keto acid. It is important because it serves both in the synthesis and degradation of amino acids.
What are the two main aminotransferases mentioned in the script and why are they significant?
-The two main aminotransferases mentioned are alanine aminotransferase (ALT) and aspartate aminotransferase (AST). They are significant because they are commonly used as markers of liver function, and elevated levels can indicate liver damage.
What role does vitamin B6 play in the transamination process?
-Vitamin B6, in the form of pyridoxal phosphate (PLP), is a coenzyme required for the function of aminotransferases. Without it, the enzymes cannot carry out transamination reactions.
What are the potential uses of the carbon skeletons derived from amino acid catabolism?
-The carbon skeletons derived from amino acid catabolism can be used for energy production, synthesis of different biological macromolecules, or converted into ketone bodies for use during prolonged fasting.
Outlines

このセクションは有料ユーザー限定です。 アクセスするには、アップグレードをお願いします。
今すぐアップグレードMindmap

このセクションは有料ユーザー限定です。 アクセスするには、アップグレードをお願いします。
今すぐアップグレードKeywords

このセクションは有料ユーザー限定です。 アクセスするには、アップグレードをお願いします。
今すぐアップグレードHighlights

このセクションは有料ユーザー限定です。 アクセスするには、アップグレードをお願いします。
今すぐアップグレードTranscripts

このセクションは有料ユーザー限定です。 アクセスするには、アップグレードをお願いします。
今すぐアップグレード5.0 / 5 (0 votes)