Ley general de los gases (Explicación y ejercicios)
Summary
TLDREste video enseña cómo resolver ejercicios utilizando la Ley General de los Gases Ideales. Se explican los pasos para encontrar el número de moles de hidrógeno en una muestra, y para calcular el volumen que ocupa el amoníaco. Se detallan los datos necesarios, la conversión de temperatura a Kelvin, la despeja de la fórmula para aislar la incógnita, y el cálculo final con los valores dados. El video invita a los espectadores a suscribirse, dar 'me gusta', comentar y volver para más contenido.
Takeaways
- 🔍 El primer ejercicio trata sobre calcular el número de moles de hidrógeno en una muestra dada utilizando la Ley General de los Gases.
- 📐 La fórmula de la Ley General de los Gases es (P × V = n × R × T), donde P es la presión, V el volumen, n el número de moles, R la constante universal de los gases y T la temperatura.
- ⚖️ Se proporcionan datos iniciales: presión de 1,24 atmósferas, volumen de 2,35 L, temperatura de 42 grados Celsius y constante R de 0,082 L·atm/K·mol.
- 🌡️ Para aplicar la Ley General de los Gases, es necesario convertir la temperatura de grados Celsius a Kelvin, sumando 273 a la temperatura dada.
- 🔢 Se despeja la fórmula para encontrar el número de moles n, resultando en n = (P × V) / (R × T).
- 🧮 Se reemplazan los valores en la fórmula despejada y se realiza el cálculo, obteniendo un resultado de 0,1111 moles de hidrógeno.
- 🔑 El segundo ejercicio se centra en hallar el volumen ocupado por 35 gramos de amoníaco a 40 grados Celsius y 3 atmósferas de presión.
- 🔄 Se repiten los pasos de obtener datos, convertir unidades (especialmente temperatura a Kelvin) y despejar la incógnita (volumen en este caso).
- 📉 Se calcula el número de moles de amoníaco a partir de su peso molecular (17 g/mol) y se obtiene que 35 gramos equivalen a 2,058 moles.
- 📏 Finalmente, se resuelve el volumen utilizando la fórmula despejada, obteniendo un volumen de 17,6 litros para los 2,058 moles de amoníaco bajo las condiciones dadas.
Q & A
¿Cuál es la Ley General de los Gases Ideales mencionada en el guion?
-La Ley General de los Gases Ideales es la ecuación \( P \times V = n \times R \times T \), donde P es la presión, V es el volumen, n es el número de moles, R es la constante universal de los gases y T es la temperatura.
¿Cuál es el primer paso al resolver ejercicios con la Ley General de los Gases Ideales según el guion?
-El primer paso es obtener los datos necesarios, que se obtienen de la fórmula de la Ley General de los Gases.
¿Cómo se convierte la temperatura de grados Celsius a Kelvin para aplicar en la Ley General de los Gases Ideales?
-Para convertir de grados Celsius a Kelvin, se suma 273 a la temperatura en grados Celsius.
¿Cuál es el segundo paso en la resolución de ejercicios con la Ley General de los Gases Ideales?
-El segundo paso es convertir los valores necesarios a las unidades correctas para poder aplicar la Ley General de los Gases, como la temperatura en Kelvin.
¿Cómo se despeja el número de moles (n) en la ecuación de la Ley General de los Gases Ideales?
-Para despejar n, se divide el producto de presión y volumen (PV) entre la constante universal (R) multiplicada por la temperatura (T).
¿Cuál es el resultado del número de moles de hidrógeno en el primer ejercicio del guion?
-El número de moles de hidrógeno es de 0,1111 moles.
¿Cuál es el segundo ejemplo tratado en el guion y qué se busca encontrar?
-El segundo ejemplo trata de encontrar el volumen ocupado por 35 gramos de amoníaco a 40 grados Celsius y 3 atmósferas.
¿Cómo se calcula el número de moles de amoníaco a partir de sus gramos moleculares?
-Para calcular el número de moles de amoníaco, se divide la cantidad en gramos (35 g) entre el peso molecular del amoníaco (17 g/mol).
¿Cuál es la constante universal de los gases (R) utilizada en el guion?
-La constante universal de los gases (R) utilizada en el guion es de 0,082 atmósferas litros por Kelvin por mol.
¿Cómo se despeja el volumen (V) en la ecuación de la Ley General de los Gases Ideales para el segundo ejemplo?
-Para despejar V, se divide el número de moles (n) multiplicado por la constante (R) y la temperatura (T) entre la presión (P).
¿Cuál es el volumen ocupado por 35 gramos de amoníaco en el segundo ejemplo del guion?
-El volumen ocupado por 35 gramos de amoníaco es de 17,6 litros.
Outlines

Cette section est réservée aux utilisateurs payants. Améliorez votre compte pour accéder à cette section.
Améliorer maintenantMindmap

Cette section est réservée aux utilisateurs payants. Améliorez votre compte pour accéder à cette section.
Améliorer maintenantKeywords

Cette section est réservée aux utilisateurs payants. Améliorez votre compte pour accéder à cette section.
Améliorer maintenantHighlights

Cette section est réservée aux utilisateurs payants. Améliorez votre compte pour accéder à cette section.
Améliorer maintenantTranscripts

Cette section est réservée aux utilisateurs payants. Améliorez votre compte pour accéder à cette section.
Améliorer maintenantVoir Plus de Vidéos Connexes

LEYES DE LOS GASES: Boyle, Charles, Ley Combinada y Ley General

[Química] 🔔Leyes de los gases 💥LEY COMBINADA🔑

Usar la ley de los gases ideales para calcular el cambio en el volumen. Ejemplo
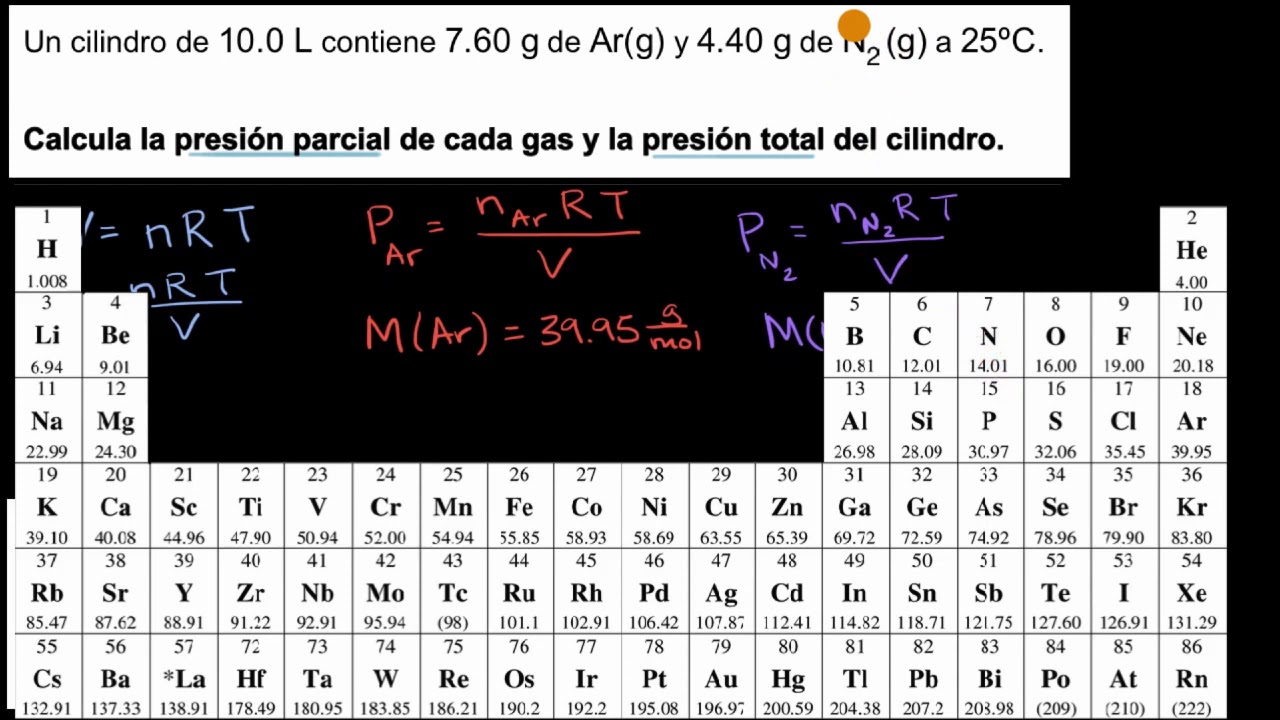
Presión parcial. Ejemplo | Khan Academy en Español

Gases | Química - Educatina

LEYES DE LOS GASES | Teoría de Gases
5.0 / 5 (0 votes)
