Ley de Dalton de las presiones parciales
Summary
TLDREl guion explica la ley de Dalton sobre las presiones parciales y resuelve un ejercicio para aplicar las fórmulas. Se describe cómo la presión total en un recipiente de gas mixto se calcula sumando las presiones parciales de cada gas, y cómo cada presión parcial se relaciona con la fracción molar del gas. Se ejemplifica con una mezcla de oxígeno y hidrógeno, calculando la presión total y parciales en un recipiente de 50 DM³ a 15°C, usando la constante de los gases ideales y las unidades correctas.
Takeaways
- 🔬 La ley de Dalton de las presiones parciales explica cómo se suman las presiones ejercidas por diferentes gases en una mezcla.
- 🧪 La presión parcial de un gas es la presión que ese gas ejercería si estuviera solo en el recipiente.
- 📏 La presión total de una mezcla de gases es igual a la suma de las presiones parciales individuales.
- 🌡️ Para aplicar la ecuación de los gases ideales en una mezcla, se debe considerar que la presión y el número de moles son totales, mientras que el volumen y la temperatura deben ser los mismos para todos los gases.
- 📐 La fórmula para calcular la presión parcial de un elemento en una mezcla es: presión parcial = presión total × fracción molar del elemento.
- 📉 La fracción molar se define como la relación entre los moles de una sustancia y los moles totales en la mezcla.
- 🔢 Para calcular la presión total en una mezcla, se utiliza la ecuación de los gases ideales: P = (nRT)/V, donde P es la presión, n es el número de moles totales, R es la constante de los gases ideales, T es la temperatura en Kelvin y V es el volumen.
- ♻️ Antes de aplicar la ecuación de los gases ideales, se deben asegurar que las unidades sean correctas, como la conversión del volumen de decímetros cúbicos a metros cúbicos y la temperatura de grados Celsius a Kelvin.
- 🧐 En el ejemplo proporcionado, se calcula la presión parcial de oxígeno y hidrógeno en una mezcla contenida en un recipiente de 50 decímetros cúbicos a 15 grados Celsius.
- 📝 Se demuestra paso a paso cómo se calculan las presiones parciales individuales de los gases en la mezcla utilizando la presión total y las fracciones moles correspondientes.
Q & A
¿Qué es la ley de Dalton de las presiones parciales?
-La ley de Dalton de las presiones parciales establece que la presión total de una mezcla de gases es igual a la suma de las presiones parciales que cada uno de los gases ejerce si estuviera solo en el mismo volumen y a la misma temperatura.
¿Cómo se representa la presión parcial en el script?
-En el script, la presión parcial se representa con dibujos que ilustran la presión que ejercen las partículas de un gas en un volumen específico, como se muestra con el gas de color verde ejerciendo una presión parcial de 30 hectopascales.
¿Cuál es la presión total en el recipiente mencionado en el guion?
-La presión total en el recipiente donde se encuentran mezclados tres gases diferentes es de 100 hectopascales.
¿Cómo se calcula la presión parcial de un gas en una mezcla?
-La presión parcial de un gas en una mezcla se calcula multiplicando la presión total por la fracción molar de ese gas, que es el número de moles de ese gas dividido por el número total de moles en la mezcla.
¿Qué es la fracción molar y cómo se calcula?
-La fracción molar es la proporción de los moles de una sustancia en relación con el total de moles en una mezcla. Se calcula dividiendo los moles de la sustancia por los moles totales de la mezcla.
¿Cuál es la relación entre la presión total y las presiones parciales según la ecuación de los gases ideales?
-Según la ecuación de los gases ideales, la presión total de una mezcla es igual a la suma de las presiones parciales de cada uno de los gases en la mezcla.
¿Qué datos son necesarios para calcular la presión total en un recipiente de gases?
-Para calcular la presión total en un recipiente de gases, se necesitan los moles totales, el volumen en metros cúbicos, la temperatura en Kelvin y la constante de los gases ideales (8,31 J/(mol·K)).
¿Cómo se convierten los decímetros cúbicos a metros cúbicos para aplicar en la ecuación de los gases ideales?
-Para convertir decímetros cúbicos a metros cúbicos, se divide el volumen en decímetros cúbicos entre 1000, ya que 1 metro cúbico es igual a 1000 decímetros cúbicos.
¿Cuál es la presión total calculada en el ejercicio del guion?
-La presión total calculada en el ejercicio del guion es de aproximadamente 52,65216 pascales.
¿Cómo se calcula la presión parcial del oxígeno y del hidrógeno en el ejercicio del guion?
-La presión parcial del oxígeno se calcula multiplicando la presión total por la fracción molar del oxígeno, que es 0,3 moles de oxígeno dividido por 1,1 moles totales. El resultado es de 14359,68 pascales. La presión parcial del hidrógeno se calcula de manera similar, resultando en 38,000,29248 pascales.
Outlines

Dieser Bereich ist nur für Premium-Benutzer verfügbar. Bitte führen Sie ein Upgrade durch, um auf diesen Abschnitt zuzugreifen.
Upgrade durchführenMindmap

Dieser Bereich ist nur für Premium-Benutzer verfügbar. Bitte führen Sie ein Upgrade durch, um auf diesen Abschnitt zuzugreifen.
Upgrade durchführenKeywords

Dieser Bereich ist nur für Premium-Benutzer verfügbar. Bitte führen Sie ein Upgrade durch, um auf diesen Abschnitt zuzugreifen.
Upgrade durchführenHighlights

Dieser Bereich ist nur für Premium-Benutzer verfügbar. Bitte führen Sie ein Upgrade durch, um auf diesen Abschnitt zuzugreifen.
Upgrade durchführenTranscripts

Dieser Bereich ist nur für Premium-Benutzer verfügbar. Bitte führen Sie ein Upgrade durch, um auf diesen Abschnitt zuzugreifen.
Upgrade durchführenWeitere ähnliche Videos ansehen

Presiones parciales de Dalton

LEY DE DALTON: PRESIONES PARCIALES (Explicación y ejercicio) | Leyes de los gases ideales

GASES LEY DE DALTON, FRACCION MOLAR, PESO MOLECULAR PROMEDIO DE UNA MEZCLA DE GASES, LEY DE AMAGAT
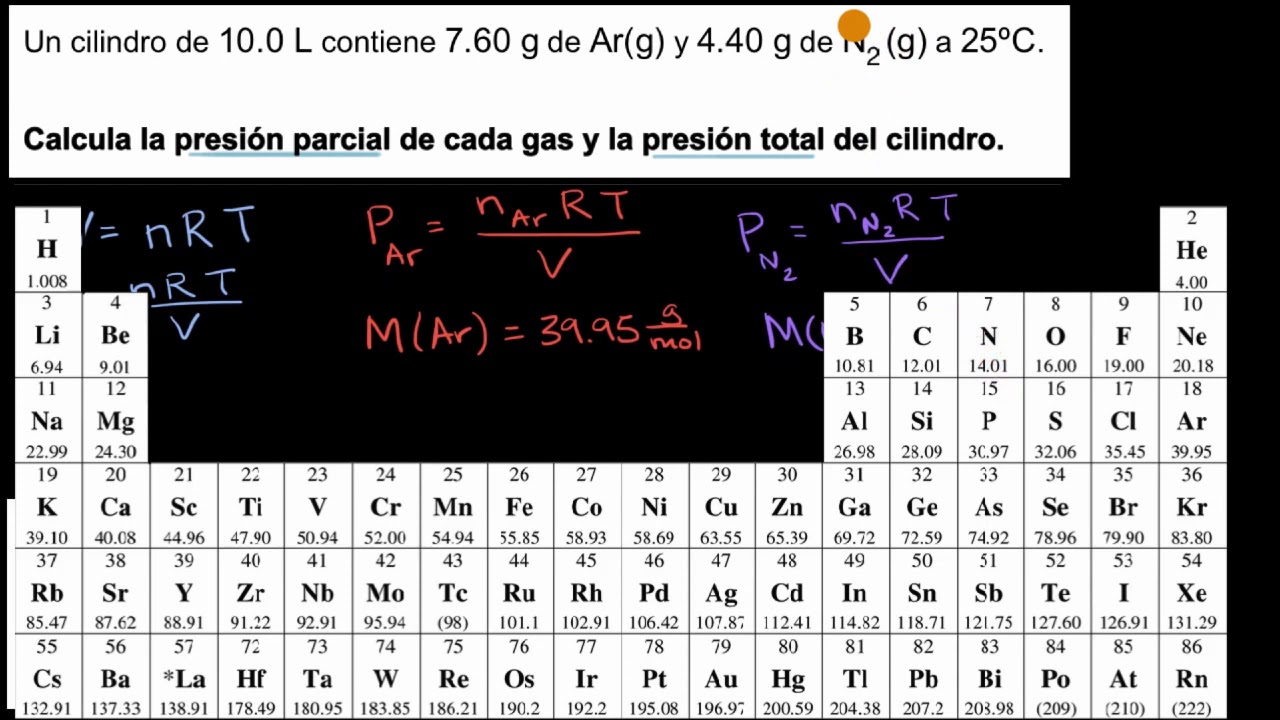
Presión parcial. Ejemplo | Khan Academy en Español

Ley de Dalton | Gases

Colisiones o choques elasticos
5.0 / 5 (0 votes)
