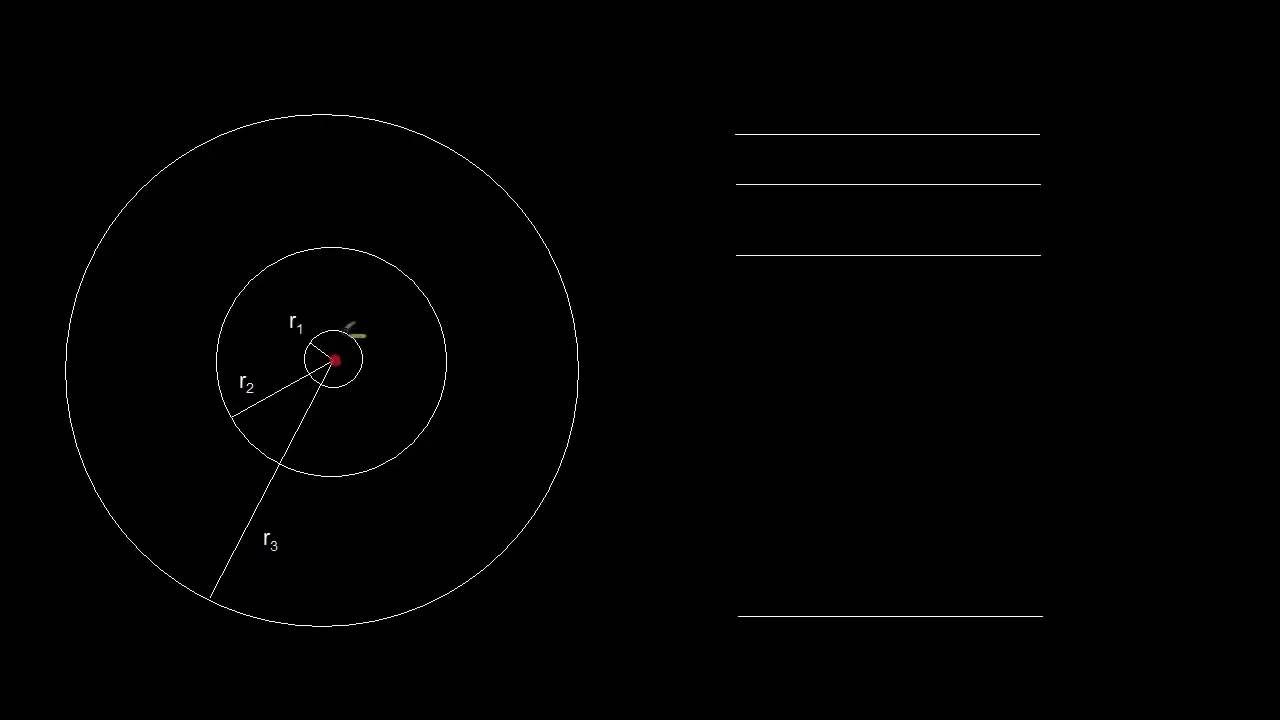
Niveles de energía en el modelo de Bohr. Deducción utilizando física
Summary
TLDREn este video, se analiza el modelo de Bohr del átomo de hidrógeno, centrándose en los niveles de energía del electrón. Se exploran conceptos como la energía cinética, la energía potencial y la energía total del electrón en su órbita alrededor del núcleo, utilizando la ley de Coulomb y la física de movimientos circulares. Se calcula la energía total en el primer nivel de energía, mostrando cómo la energía en niveles más altos se cuantiza. Al final, se destaca cómo estos niveles de energía cuantizados explican varios fenómenos atómicos, con planes para un análisis más profundo en próximos videos.
Takeaways
- 😀 La energía cinética del electrón se calcula utilizando la fórmula 1/2 * m * v², donde m es la masa del electrón y v su velocidad.
- 😀 El electrón en el modelo de Bohr se mueve alrededor del núcleo del átomo de hidrógeno debido a la fuerza eléctrica que ejerce el protón en el núcleo.
- 😀 La fuerza eléctrica que mantiene al electrón en su órbita se calcula usando la ley de Coulomb, que depende de la carga de las partículas y la distancia entre ellas.
- 😀 La aceleración centrípeta del electrón se utiliza para calcular la magnitud de la fuerza eléctrica que lo mantiene en su trayectoria circular alrededor del núcleo.
- 😀 La expresión de la energía cinética del electrón se obtiene al igualar la fuerza eléctrica a la masa por la aceleración centrípeta, resultando en 1/2 * m * v² = K * e² / r.
- 😀 La energía potencial eléctrica del electrón se calcula con la fórmula -K * e² / r, donde el signo negativo refleja que la energía potencial es negativa cuando el electrón está atado al núcleo.
- 😀 La energía total del electrón es la suma de la energía cinética y la energía potencial, lo que da como resultado una fórmula para la energía total: E_total = -1/2 * K * e² / r.
- 😀 Cuando el radio de la órbita del electrón es igual a R1 (radio de Bohr), la energía total en el nivel fundamental es -2.17 * 10⁻¹⁸ J.
- 😀 La fórmula generalizada para la energía en cualquier nivel de energía n es E_n = -1/2 * K * e² / R_n, donde R_n es el radio del nivel energético n.
- 😀 La energía total de un electrón en el modelo de Bohr es cuantizada, lo que significa que solo puede tomar valores discretos dependiendo del número cuántico n, lo que ayuda a explicar los niveles de energía cuantizados del átomo.
Q & A
¿Qué es la energía cinética del electrón en el modelo de Bohr?
-La energía cinética del electrón es igual a 1/2 * m * v², donde m es la masa del electrón y v es su velocidad. Este valor representa la energía asociada al movimiento del electrón mientras gira alrededor del núcleo.
¿Cómo se calcula la fuerza eléctrica en el modelo de Bohr?
-La fuerza eléctrica se calcula usando la Ley de Coulomb: F = k * q1 * q2 / r², donde k es la constante de Coulomb, q1 y q2 son las cargas del protón y el electrón, y r es la distancia entre ellos.
¿Qué relación existe entre la fuerza centrípeta y la fuerza eléctrica en el modelo de Bohr?
-La fuerza eléctrica que atrae al electrón hacia el núcleo es la misma que la fuerza centrípeta que mantiene al electrón en su órbita circular. Estas dos fuerzas son iguales en magnitud, pero opuestas en dirección.
¿Cuál es la expresión para la energía cinética del electrón?
-La expresión para la energía cinética del electrón es 1/2 * k * e² / r, donde k es la constante de Coulomb, e es la carga elemental, y r es la distancia entre el electrón y el núcleo.
¿Qué fórmula se utiliza para calcular la energía potencial eléctrica del electrón?
-La energía potencial eléctrica se calcula con la fórmula: U = - k * e² / r, donde k es la constante de Coulomb, e es la carga elemental, y r es la distancia entre el electrón y el núcleo.
¿Por qué la energía total del electrón es negativa en el modelo de Bohr?
-La energía total del electrón es negativa porque la energía potencial es negativa y la energía cinética es positiva, pero la magnitud de la energía cinética es mayor que la de la energía potencial, lo que lleva a una energía total negativa. Esto indica que el electrón está en un estado ligado al núcleo.
¿Cómo se calcula la energía total en el modelo de Bohr?
-La energía total se calcula sumando la energía cinética y la energía potencial. La expresión final es E_total = - 1/2 * k * e² / r, lo que nos da la energía asociada con el electrón en su órbita.
¿Qué es el estado fundamental en el modelo de Bohr y cómo se calcula su energía?
-El estado fundamental es el nivel de energía más bajo en el que se encuentra el electrón. Su energía se calcula usando la fórmula E1 = - 2.17 * 10^-18 J, con r1 siendo la distancia de 5.3 * 10^-11 m, correspondiente al primer nivel de energía.
¿Cómo se generaliza la fórmula para la energía total en niveles de energía superiores?
-La fórmula generalizada para la energía total en cualquier nivel de energía n es: E_n = - 1/2 * k * e² / r_n, donde r_n es el radio en el nivel n. Esto nos permite calcular la energía en cualquier nivel cuántico del átomo de hidrógeno.
¿Por qué la energía en el modelo de Bohr es cuantizada?
-La energía es cuantizada porque el electrón solo puede existir en ciertos niveles de energía discretos. Cada nivel de energía se corresponde con una órbita específica alrededor del núcleo, y la energía del electrón solo puede tomar valores específicos relacionados con estos niveles.
Outlines

This section is available to paid users only. Please upgrade to access this part.
Upgrade NowMindmap

This section is available to paid users only. Please upgrade to access this part.
Upgrade NowKeywords

This section is available to paid users only. Please upgrade to access this part.
Upgrade NowHighlights

This section is available to paid users only. Please upgrade to access this part.
Upgrade NowTranscripts

This section is available to paid users only. Please upgrade to access this part.
Upgrade Now5.0 / 5 (0 votes)