Hypertonisch - Hypotonisch - Isotonisch [Konzentrationen von Lösungen + Klausurtipp] - [Biologie]
Summary
TLDRIn diesem Video werden die Begriffe Hypertonie, Hypotonie und Isotonie erklärt, die verwendet werden, um die Konzentration von Lösungen im Zusammenhang mit Osmose zu beschreiben. Es wird erklärt, wie Lösungen mit unterschiedlicher Konzentration durch eine Membran getrennt sind und wie Wasser über Osmose in die Lösung mit der höheren Konzentration diffundiert, um ein Gleichgewicht zu erreichen. Der Unterschied zwischen hypertonen, hypotonen und isotonen Lösungen wird detailliert erläutert, und wichtige Hinweise für Klausuren zu diesen Begriffen werden gegeben.
Takeaways
- 😀 In diesem Video geht es um die Begriffe Hypertonie, Hypotonie und Isotonie, die verwendet werden, um die Konzentration zwischen zwei Lösungen zu beschreiben.
- 😀 Diese Begriffe werden häufig im Zusammenhang mit der Osmose verwendet, um die Unterschiede in der osmotischen Konzentration zu erklären.
- 😀 Eine isotonische Lösung hat die gleiche Konzentration an gelösten Stoffen wie das Vergleichsmedium, zum Beispiel der intrazelluläre Raum im Vergleich zum extrazellulären Raum.
- 😀 Osmotische Konzentration bezieht sich auf die Gesamtzahl der gelösten Teilchen in einer Lösung, die miteinander verglichen werden.
- 😀 In einer isotonischen Lösung gibt es die gleiche Anzahl gelöster Teilchen pro Liter wie im Vergleichsmedium.
- 😀 Hypertonie bedeutet, dass eine Lösung eine höhere Konzentration an gelösten Teilchen hat als das Vergleichsmedium.
- 😀 Hypotonie beschreibt eine Lösung mit einer geringeren Konzentration an gelösten Teilchen im Vergleich zum Medium, wie im Fall des intra- versus extrazellulären Raums.
- 😀 Wasser diffundiert immer in das hypertonische Medium, um den Konzentrationsunterschied der gelösten Teilchen auszugleichen – dieser Prozess wird als Osmose bezeichnet.
- 😀 Wenn der Konzentrationsunterschied umkehrt, diffundiert Wasser aus der Zelle hinaus, wenn der intrazelluläre Raum nun hypotonisch im Vergleich zum extrazellulären Raum ist.
- 😀 In Klausuren ist es wichtig, bei der Anwendung der Begriffe Hypertonie und Hypotonie immer anzugeben, welches Medium verglichen wird, um die richtige Antwort zu gewährleisten.
Q & A
Was bedeutet der Begriff 'isotonische Lösung'?
-Eine isotonische Lösung hat die gleiche Konzentration an gelösten Stoffen wie das Vergleichsmedium, zum Beispiel der Bereich außerhalb der Zelle. Dadurch findet keine Netto-Wasserbewegung zwischen der Zelle und ihrer Umgebung statt.
Was passiert, wenn eine Zelle in einer hypertonischen Lösung platziert wird?
-In einer hypertonischen Lösung wird Wasser aus der Zelle herausdiffundieren, da die Konzentration an gelösten Stoffen im Außenbereich höher ist. Dies führt dazu, dass die Zelle schrumpft.
Was bedeutet der Begriff 'hypotonische Lösung'?
-Eine hypotonische Lösung hat eine geringere Konzentration an gelösten Stoffen im Vergleich zu der Zelle oder einem anderen Vergleichsmedium. In diesem Fall diffundiert Wasser in die Zelle, wodurch sie anschwellen und möglicherweise platzen kann.
Wie beeinflusst die semipermeable Membran die Osmose?
-Die semipermeable Membran lässt nur bestimmte Substanzen durch, in der Regel Wasser, während sie andere gelöste Stoffe blockiert. Dies führt dazu, dass Wasser in Richtung der höheren Konzentration an gelösten Stoffen diffundiert, um die Konzentrationsunterschiede auszugleichen.
Was ist der Hauptmechanismus, der die Wasserbewegung bei der Osmose antreibt?
-Der Hauptmechanismus, der die Wasserbewegung bei der Osmose antreibt, ist der Konzentrationsunterschied der gelösten Stoffe zwischen den beiden Seiten der Membran. Wasser bewegt sich vom Bereich niedrigerer Konzentration zu dem mit höherer Konzentration.
Warum diffundiert Wasser immer ins hypertonische Medium?
-Wasser diffundiert immer ins hypertonische Medium, weil dort die Konzentration an gelösten Teilchen höher ist. Um den Konzentrationsunterschied auszugleichen, bewegt sich Wasser in Richtung des Mediums mit der höheren Konzentration an gelösten Stoffen.
Wie würde sich der osmotische Fluss ändern, wenn sich das Verhältnis der gelösten Stoffe innerhalb der Zelle und im Außenmedium umkehrt?
-Wenn sich das osmotische Verhältnis umkehrt, zum Beispiel wenn der innere Zellraum weniger gelöste Stoffe enthält als das Außenmedium, würde Wasser aus der Zelle hinaus diffundieren, um die Konzentration im Vergleichsmedium auszugleichen.
Was bedeutet es, dass die Begriffe hypertonisch und hypotonisch relative Begriffe sind?
-Die Begriffe hypertonisch und hypotonisch sind relativ, weil sie immer die Konzentration von gelösten Stoffen im Vergleich zu einem anderen Medium beschreiben. Eine Lösung ist nur dann hypertonisch oder hypotonisch, wenn sie in Bezug auf eine andere Lösung bewertet wird.
Wie kann man in einer Klausur die Konzentration einer Lösung korrekt als hypertonisch oder hypotonisch beschreiben?
-Um in einer Klausur die Konzentration korrekt zu beschreiben, muss man immer angeben, mit welchem Medium verglichen wird. Zum Beispiel: Wenn das Extrazellulärmedium hypothetisch ist, muss man ableiten, dass das intrazelluläre Medium hypertonisch ist.
Welche Auswirkungen hat es, wenn eine Zelle in einer Lösung mit einer höheren osmotischen Konzentration als das Zellinnere platziert wird?
-Wenn eine Zelle in einer Lösung mit einer höheren osmotischen Konzentration als das Zellinnere platziert wird (hypertonische Lösung), wird Wasser aus der Zelle diffundieren, wodurch die Zelle schrumpft.
Outlines

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифMindmap

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифKeywords

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифHighlights

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифTranscripts

Этот раздел доступен только подписчикам платных тарифов. Пожалуйста, перейдите на платный тариф для доступа.
Перейти на платный тарифПосмотреть больше похожих видео

Stärke von Säuren und Basen verstehen| Ks,Kb,pKs,pKb und Berechnungen

Übungsaufgabe - Lambert-beer'sches Gesetz: Konzentration berechnen | Physik - Grundlagen
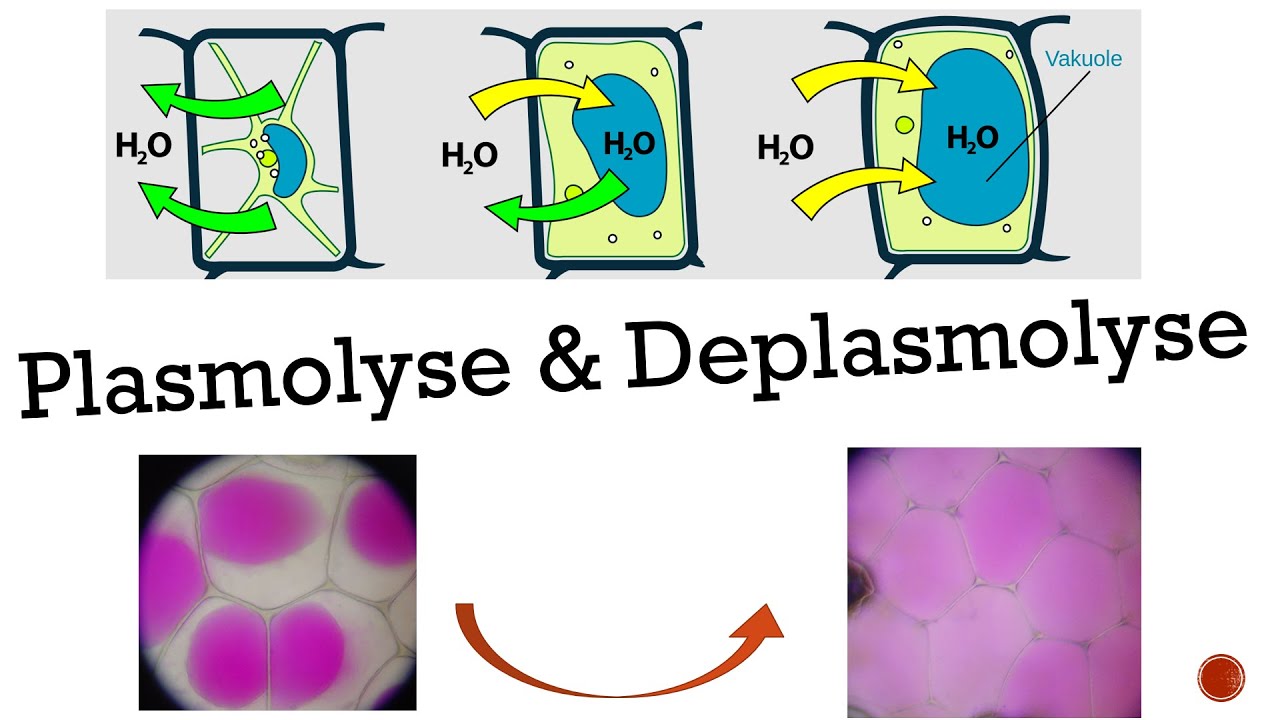
Plasmolyse & Deplasmolyse [Biologie, Oberstufe]

Diffusion und Osmose - Wie geht's?

Richtig Links abbiegen - So machst Du keine Fehler mehr (Teil 2) - Führerschein

past perfect progressive - einfach erklärt | Einfach Englisch
5.0 / 5 (0 votes)
