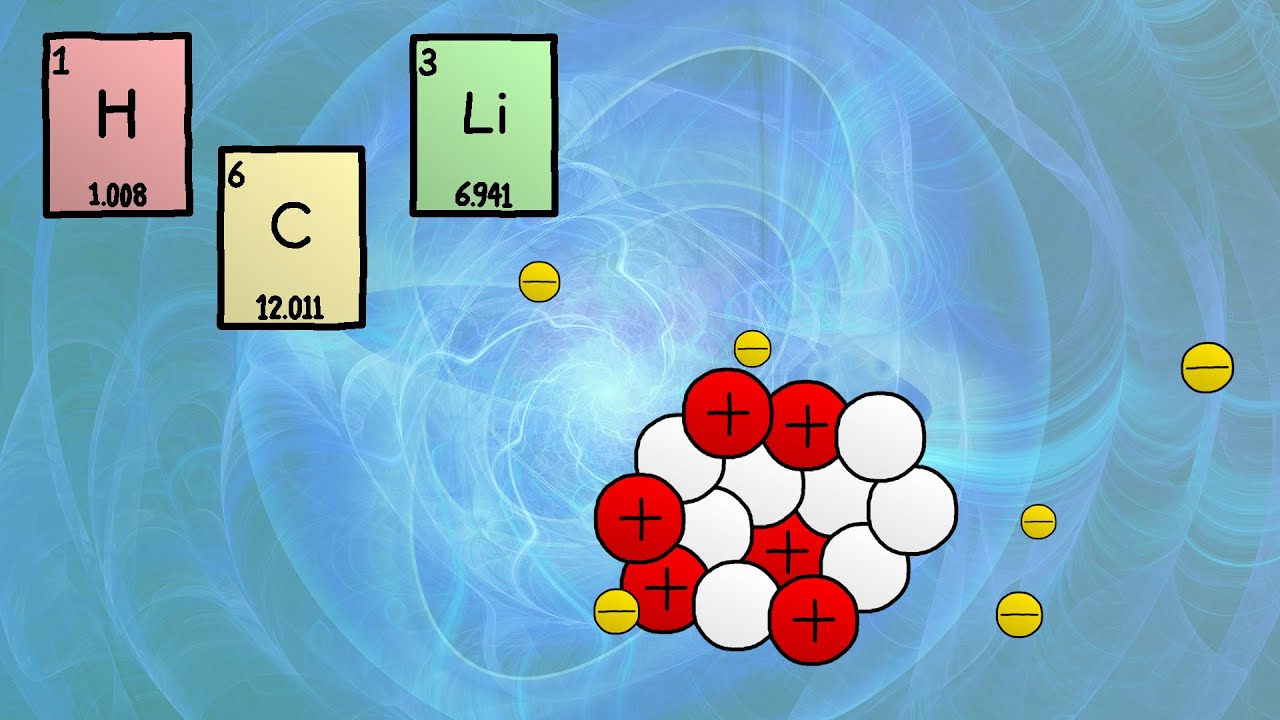
Isótopos, número de masa, número atómico, protones, electrones, neutrones, tabla de isótopos
Summary
TLDREste video explica los isótopos, que son átomos de un mismo elemento con diferente número de neutrones. Se enseña cómo representarlos mediante el símbolo químico, el número de masa (suma de protones y neutrones) y el número atómico (número de protones). A través de ejemplos como el hidrógeno y el carbono, se ilustra cómo calcular los neutrones y cómo los isótopos se representan en tablas. Además, se abordan los conceptos de isotopía y su uso en la datación de fósiles. El video proporciona una visión clara y práctica de cómo trabajar con isótopos en química.
Takeaways
- 😀 Los isótopos son átomos del mismo elemento químico que tienen diferente número de neutrones.
- 😀 El número atómico (Z) representa la cantidad de protones en un átomo, mientras que el número másico (A) es la suma de protones y neutrones.
- 😀 Un átomo neutro tiene el mismo número de protones y electrones.
- 😀 La masa del átomo está concentrada en el núcleo, que contiene protones y neutrones.
- 😀 Los electrones tienen carga negativa, pero su masa es mucho menor que la de los protones y neutrones.
- 😀 El hidrógeno tiene tres isótopos: protio (H-1), deuterio (H-2) y tritio (H-3), que difieren en el número de neutrones.
- 😀 El carbono tiene tres isótopos representativos: carbono-12, carbono-13 y carbono-14, siendo este último útil para la datación de fósiles.
- 😀 El número de neutrones de un isótopo se puede encontrar restando el número atómico del número másico.
- 😀 En algunos ejercicios, se proporciona un cuadro con información incompleta sobre isótopos y se debe calcular la información faltante.
- 😀 Un ejemplo práctico de cálculo de isótopos es el bromo-35, donde el número de neutrones se calcula restando el número atómico del número másico (80 - 35 = 45).
Q & A
¿Qué son los isótopos?
-Los isótopos son átomos de un mismo elemento químico que tienen el mismo número de protones pero un número diferente de neutrones, lo que da como resultado diferentes números de masa.
¿Cómo se representa un isótopo?
-Un isótopo se representa con el símbolo del elemento químico, el número de masa (A) en la parte superior y el número atómico (Z) en la parte inferior.
¿Qué es el número de masa (A)?
-El número de masa (A) es la suma de los protones y los neutrones en el núcleo del átomo.
¿Qué representa el número atómico (Z)?
-El número atómico (Z) representa el número de protones en un átomo y determina el elemento químico al que pertenece.
En un átomo neutro, ¿cómo se relacionan los protones y los electrones?
-En un átomo neutro, el número de protones es igual al número de electrones, ya que deben balancear las cargas para que no haya carga neta.
¿Dónde se encuentran los protones, neutrones y electrones en un átomo?
-Los protones y neutrones se encuentran en el núcleo del átomo, mientras que los electrones se encuentran en la periferia o alrededor del núcleo.
¿Cuál es la diferencia en masa entre un electrón y un neutrón?
-El electrón tiene una masa mucho menor que un neutrón; de hecho, se necesitarían aproximadamente 2000 electrones para igualar la masa de un neutrón.
¿Cuáles son los tres isótopos del hidrógeno y cómo se diferencian?
-Los tres isótopos del hidrógeno son: el protio (H-1, con 1 protón y 0 neutrones), el deuterio (H-2, con 1 protón y 1 neutrón) y el tritio (H-3, con 1 protón y 2 neutrones).
¿Qué es la abundancia de los isótopos en la naturaleza?
-La abundancia de los isótopos varía según el elemento. Por ejemplo, el protio es el isótopo más abundante del hidrógeno, mientras que el tritio es mucho más raro.
¿Cómo se utilizan los isótopos del carbono en datación?
-El carbono tiene tres isótopos (C-12, C-13, y C-14), siendo el C-14 utilizado en la datación por radiocarbono para determinar la edad de fósiles y restos orgánicos.
¿Cómo se calcula el número de neutrones en un isótopo?
-El número de neutrones se calcula restando el número atómico (Z) del número de masa (A). Por ejemplo, en el isótopo del carbono C-14, el número de neutrones es 14 - 6 = 8.
¿Qué información adicional proporciona un cuadro de isótopos?
-Un cuadro de isótopos puede proporcionar información como el número atómico (Z), el número de masa (A), el número de protones, neutrones y electrones, permitiendo calcular valores faltantes o confirmar propiedades del isótopo.
Outlines

Dieser Bereich ist nur für Premium-Benutzer verfügbar. Bitte führen Sie ein Upgrade durch, um auf diesen Abschnitt zuzugreifen.
Upgrade durchführenMindmap

Dieser Bereich ist nur für Premium-Benutzer verfügbar. Bitte führen Sie ein Upgrade durch, um auf diesen Abschnitt zuzugreifen.
Upgrade durchführenKeywords

Dieser Bereich ist nur für Premium-Benutzer verfügbar. Bitte führen Sie ein Upgrade durch, um auf diesen Abschnitt zuzugreifen.
Upgrade durchführenHighlights

Dieser Bereich ist nur für Premium-Benutzer verfügbar. Bitte führen Sie ein Upgrade durch, um auf diesen Abschnitt zuzugreifen.
Upgrade durchführenTranscripts

Dieser Bereich ist nur für Premium-Benutzer verfügbar. Bitte führen Sie ein Upgrade durch, um auf diesen Abschnitt zuzugreifen.
Upgrade durchführenWeitere ähnliche Videos ansehen
5.0 / 5 (0 votes)