Las propiedades periódicas de los elementos
Summary
TLDREste script ofrece una visión detallada de las propiedades periódicas de los elementos químicos. Se comienza con una revisión de la organización de los elementos en la tabla periódica, destacando la importancia de los grupos y periodos. Se profundiza en las relaciones de tamaño, como el radio atómico, y las relaciones de energía, incluyendo el potencial de ionización y la afinidad eléctrica. La electronegatividad es un tema central, que se relaciona con la capacidad de los átomos para atraer electrones en una molécula. Se ilustra con ejemplos cómo la electronegatividad influye en la formación de enlaces químicos, y cómo las diferencias en electronegatividad determinan si un enlace es covalente no polar, polar o iónico. El script concluye con una breve mención de los enlaces químicos y la transferencia electrónica. Finalmente, se ofrece un resumen visual de cómo estas propiedades varían a lo largo de la tabla periódica, destacando el aumento del carácter metálico y la disminución del carácter no metálico a medida que se desplaza desde abajo hacia arriba y de derecha a izquierda en la tabla.
Takeaways
- 🔬 Los elementos en la tabla periódica están organizados según su número atómico y se agrupan en grupos y periodos.
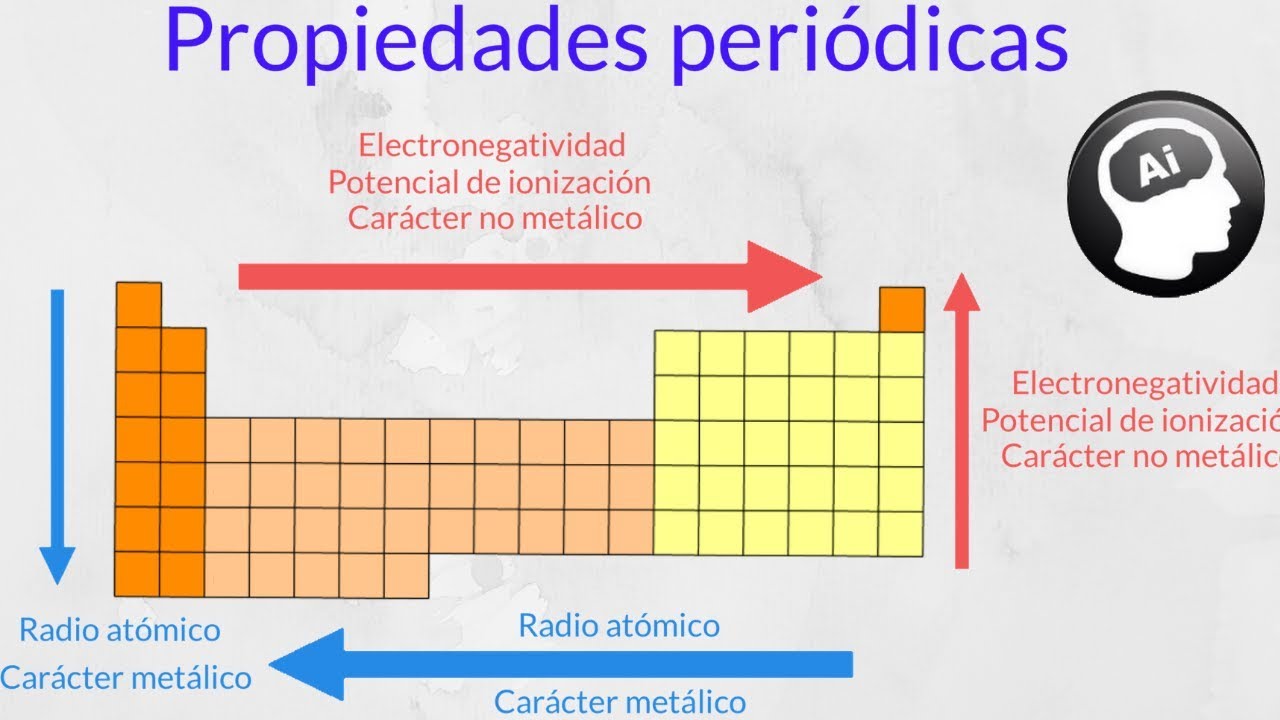
- 📊 El radio atómico es la distancia desde el núcleo de un átomo hasta su electrón más lejano y aumenta de arriba hacia abajo y de derecha a izquierda en la tabla periódica.
- ⬆️ La energía de ionización, que es la energía necesaria para separar un electrón de un átomo en estado gaseoso, aumenta en cada período de izquierda a derecha y en cada grupo de abajo hacia arriba.
- 🔋 La afinidad electrónica, que es la energía liberada cuando un átomo gaseoso captura un electrón, tiene un comportamiento similar al potencial de ionización en la tabla periódica.
- ⚖️ La electronegatividad es la capacidad de un átomo para atraer electrones cuando forma una molécula, y aumenta en cada grupo de abajo hacia arriba y en cada período de izquierda a derecha.
- 🤝 La diferencia de electronegatividad entre dos átomos determina el tipo de enlace químico que forman: covalente no polar, covalente polar o iónico.
- 👥 Los átomos de sodio y cloro tienen una gran diferencia de electronegatividad, lo que lleva a una transferencia electrónica y formación de un enlace iónico.
- 💧 Los átomos de hidrógeno y nitrógeno tienen una diferencia de electronegatividad menor, lo que resulta en enlaces covalentes.
- 📉 El carácter metálico disminuye de arriba hacia abajo y de derecha a izquierda en la tabla periódica.
- 📈 El carácter no metálico aumenta de la misma manera que el carácter metálico pero en el sentido opuesto en la tabla periódica.
- 🔗 La electronegatividad y la diferencia de electronegatividad son fundamentales para entender la química de enlaces y la polaridad molecular.
Q & A
¿Cómo se organizan los elementos en la tabla periódica?
-Los elementos se organizan en la tabla periódica según su número atómico, en grupos y periodos, que son columnas verticales y filas horizontales respectivamente.
¿Qué es el radio atómico y cómo se define?
-El radio atómico es la distancia existente desde el núcleo de un átomo hasta su electrón más lejano. Se mide en función de la distancia del núcleo a su capa electrónica más externa.
¿Cómo varía el radio atómico en la tabla periódica?
-El radio atómico aumenta de arriba hacia abajo y de derecha hacia izquierda en la tabla periódica, con excepciones como los gases nobles.
¿Qué es el potencial de ionización y cómo se comporta en la tabla periódica?
-El potencial de ionización es la energía necesaria para separar un electrón de un átomo en estado gaseoso. Aumenta de izquierda a derecha en cada período y de abajo hacia arriba en cada grupo.
¿Qué es la afinidad eléctrica y cómo se relaciona con el potencial de ionización?
-La afinidad eléctrica es la energía liberada por un átomo gaseoso al captar un electrón. Su comportamiento en la tabla periódica es similar al del potencial de ionización, aumentando en cada período y grupo.
¿Qué es la electronegatividad y cómo se mide?
-La electronegatividad es la medida de la capacidad de un átomo para atraer electrones al formar una molécula química. Se mide en una escala numérica y varía en la tabla periódica siguiendo un patrón similar al del potencial de ionización y la afinidad electrónica.
¿Cómo se forman los enlaces químicos en función de la electronegatividad?
-La diferencia de electronegatividad entre dos átomos determina el tipo de enlace químico que se forma. Un diferencia menor o igual a 0.4 indica un enlace covalente no polar, entre 0.5 y 1.7 un enlace covalente polar, y mayor a 1.7 un enlace iónico.
¿Cómo varía el carácter metálico en la tabla periódica?
-El carácter metálico aumenta de arriba hacia abajo y disminuye de derecha a izquierda en la tabla periódica. Los elementos más metálicos se encuentran en el bloque inferior izquierdo, mientras que los más no metálicos, y por lo tanto más electro negativos, se encuentran en el superior derecho.
¿Cuál es el elemento más electro negativo en la tabla periódica?
-El elemento más electro negativo en la tabla periódica es el flúor, con un valor de electronegatividad aproximadamente de 3.9.
¿Cómo se relacionan las propiedades periódicas con las tendencias en la tabla periódica?
-Las propiedades periódicas, como el radio atómico, el potencial de ionización y la electronegatividad, aumentan o disminuyen de acuerdo con las posiciones de los elementos en la tabla periódica, reflejando tendencias periódicas relacionadas con su estructura electrónica.
¿Por qué es importante entender las propiedades periódicas de los elementos?
-El entendimiento de las propiedades periódicas es crucial para predecir el comportamiento de los elementos en reacciones químicas, para diseñar materiales y compuestos con propiedades específicas, y para la comprensión fundamental de la química.
¿Cómo se pueden compartir los electrones en un enlace químico?
-Los electrones se pueden compartir de manera igual entre átomos de electronegatividad similar, formando enlaces covalentes no polares, o de manera desigual si hay una diferencia de electronegatividad, formando enlaces covalentes polares o iónicos.
Outlines

هذا القسم متوفر فقط للمشتركين. يرجى الترقية للوصول إلى هذه الميزة.
قم بالترقية الآنMindmap

هذا القسم متوفر فقط للمشتركين. يرجى الترقية للوصول إلى هذه الميزة.
قم بالترقية الآنKeywords

هذا القسم متوفر فقط للمشتركين. يرجى الترقية للوصول إلى هذه الميزة.
قم بالترقية الآنHighlights

هذا القسم متوفر فقط للمشتركين. يرجى الترقية للوصول إلى هذه الميزة.
قم بالترقية الآنTranscripts

هذا القسم متوفر فقط للمشتركين. يرجى الترقية للوصول إلى هذه الميزة.
قم بالترقية الآنتصفح المزيد من مقاطع الفيديو ذات الصلة
5.0 / 5 (0 votes)